✒️مقدمه
استرین اکو یک روش پیشرفته در اکوکاردیوگرافی است که بهجای تکیه صرف بر تغییرات حجمی یا درصد تخلیه (EF؛ Ejection Fraction، درصد تخلیه بطن چپ یا کسرجهشی) به تغییر شکل (استرین؛ deformation) بافت میوکارد میپردازد و بنابراین اطلاعات دقیقتری درباره عملکرد مکانیکی عضله قلب ارائه میدهد.
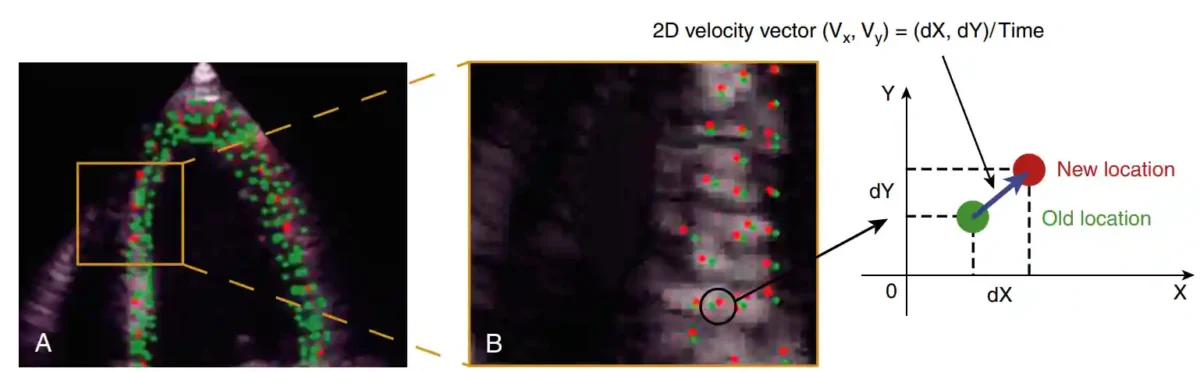
در عمل معمولاً از Speckle‑Tracking Echocardiography (ردیابی لکهها؛ الگوریتمی که الگوهای ریز تصویری را دنبال میکند) استفاده میشود؛ نرمافزار نقاط ریز (speckles) در تصاویر دوبعدی را دنبال کرده و بر اساس جابجایی این نقاط منحنیهای استرین برای نواحی مختلف میوکارد تولید میکند که امکان تحلیل موضعی عملکرد را فراهم میسازد.
یکی از شاخصهای کلیدی در این روش GLS است که به صورت Global Longitudinal Strain (کشش طولی کلی) گزارش میشود؛ GLS معمولاً به شکل درصد منفی بیان میشود (مثلاً −۱۸% تا −۲۲% در شرایط طبیعی) و کاهش مقدار مطلق آن میتواند نشاندهنده اختلال عملکرد طولی بطن چپ باشد.
تفاوت اساسی استرین با روشهای سنتی مانند EF این است که EF تغییرات کلی حجم را نشان میدهد، اما استرین میتواند اختلالات موضعی و زیر بالینی را پیش از افت قابلتوجه EF آشکار کند؛ به همین دلیل در تشخیص زودرس آسیب میوکارد و پایش تغییرات عملکردی حساستر است.
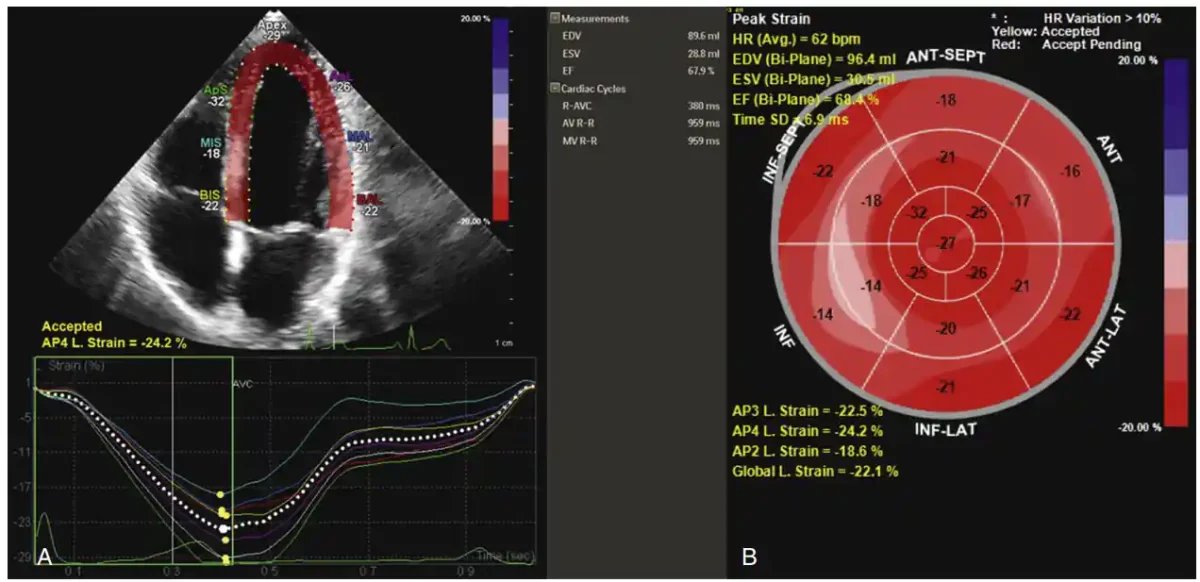
خروجیهای استرین معمولاً شامل نقشههای رنگی (strain maps)، منحنیهای زمانی برای هر بخش (segmental strain؛ استرین بخشبندیشده) و مقادیر عددی است که به پزشک کمک میکند نواحی با عملکرد ضعیف یا نامتوازن را شناسایی کند و روند تغییرات را در پیگیریهای بعدی کمّی کند.
کاربردهای بالینی استرین گسترده است؛ از پایش کاردیوکسیکوتوکسیته (cardiotoxicity؛ آسیب قلبی ناشی از داروهای شیمیدرمانی) در بیماران تحت شیمیدرمانی گرفته تا ارزیابی کاردیومیوپاتیها، تشخیص نواحی ایسکمیک و پیگیری پاسخ به درمان؛ در بسیاری از موارد تغییرات GLS میتواند هشدار اولیه برای مداخله محافظتی باشد.
مزیت مهم استرین، کمّی و تکرارپذیر بودن آن نسبت به قضاوت چشمی است، اما محدودیتهایی نیز وجود دارد: کیفیت تصویر (image quality) و تفاوت بین سازندگان دستگاه و نرمافزارها (vendor variability) میتواند باعث اختلاف در مقادیر شود، بنابراین بهتر است پیگیریها با همان دستگاه یا همان نرمافزار انجام شود یا از مقادیر مرجع سازنده استفاده گردد.
استرین مکمل روشهای دیگر اکو مانند Doppler (داپلر؛ روش اندازهگیری جریان خون و سرعت) و اندازهگیریهای حجمی است؛ ترکیب این اطلاعات تصویر کاملتری از عملکرد همودینامیک و مکانیک قلب فراهم میآورد و به تصمیمگیری بالینی دقیقتر کمک میکند.
برای اجرای صحیح استرین، ثبت نماهای استاندارد مانند AP4 (آپیکال چهارحفرهای) و PLAX (پاراسترنال طولی) با کیفیت مناسب ضروری است تا الگوریتم ردیابی لکهها بتواند بهدرستی کار کند؛ همچنین اپراتور باید با پارامترهای نرمافزار و نحوه قرار دادن نقاط مرجع آشنا باشد تا نتایج قابلاعتماد بهدست آید.
در تفسیر بالینی، نتایج استرین باید همراه با تصویر بالینی بیمار، EF، یافتههای داپلر و سایر آزمایشها بررسی شود؛ کاهش کوچک در GLS بهتنهایی همیشه نشاندهنده بیماری جدی نیست، اما در زمینه بالینی مناسب میتواند نیاز به پیگیری، تغییر درمان یا مشاوره تخصصی کاردیولوژی را مطرح کند.
⚒️مفاهیم پایه فیزیکی
استرین اکو روشی در اکوکاردیوگرافی است که بهجای اندازهگیری صرفاً تغییرات حجمی قلب، تغییر شکل (strain؛ میزان کشیدگی یا فشردگی) بافت میوکارد را کمّی میکند. این تغییر شکل نشان میدهد هر بخش از عضله قلب در طول سیکل قلبی چقدر منقبض یا کشیده میشود و بنابراین اطلاعاتی درباره عملکرد مکانیکی میوکارد میدهد که فراتر از آنچه درصد تخلیه (EF) نشان میدهد است. (Oxford Academic Springer). در استرین اکوکاردیوگرافی، هدف اندازهگیری تغییر شکل (strain) و سرعت تغییر شکل (strain rate) بافت میوکارد است تا عملکرد مکانیکی قلب را دقیقتر و موضعیتر از معیارهای حجمی سنتی مانند EF ارزیابی کنیم. این روش اکنون در راهنماها و کاربردهای بالینی پذیرفته شده و برای پایش کاردیوکسیکوتوکسیته (مصموم شدن بافتهای قلبی)، تشخیص زودرس کاردیومیوپاتی و ارزیابی ایسکمی کاربردی است.
📏مفهوم استرین
استرین یا کرنش(Strain) یعنی «تغییر شکل نسبی» بافت؛ دقیقتر بگوییم، نسبت تغییر طول یک قطعه از عضله قلب نسبت به طول اولیهاش. اگر یک نوار لاستیکی را در نظر بگیریم، وقتی آن را میکشیم طولش افزایش مییابد؛ نسبت افزایش طول به طول اولیه همان استرین است. در قلب، در زمان انقباض طول بعضی الیاف کوتاه میشود (استرین منفی در جهت طولی) و در زمان دیاستول ممکن است همان ناحیه دوباره طولانی شود. فرمول ساده و کاربردی برای استرین خطی این است:
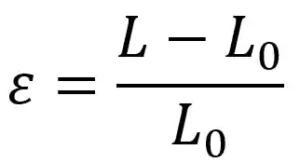
که در آن (L۰) طول اولیه (معمولاً طول در ابتدای سیکل مرجع، مثل ابتدای دیاستول) و (L) طول در لحظه مورد نظر است. اگر (ɛ) منفی باشد یعنی بافت کوتاه شده؛ اگر مثبت باشد یعنی طولانی یا ضخیم شده است (مثلاً در جهت شعاعی دیواره).
برای درک بهتر، فرض کنید یک خطکش ۱۰ سانتیمتری روی دیواره قلب قرار گرفته. در ابتدای دیاستول طول آن ۱۰ سانتیمتر است. در اوج سیستول طولش به ۸ سانتیمتر میرسد. استرین برابر است با ((۸-۱۰)/۱۰ = -۰.۲) یعنی (-۲۰%). این عدد نشان میدهد آن ناحیه ۲۰٪ کوتاهتر شده است — در قلب، چنین مقدار منفی طولی معمولاً طبیعی و نشاندهنده انقباض خوب است.
نرخ استرین (Strain Rate) سرعت تغییر همین استرین در واحد زمان است؛ یعنی چقدر سریع آن ناحیه از عضله از طول (L۰) به (L) میرسد. اگر استرین مثل «فاصلهای که ماشین طی میکند» باشد، نرخ استرین مثل «سرعت ماشین» است. فرمول ساده برای نرخ استرین به صورت مشتق زمانی است:
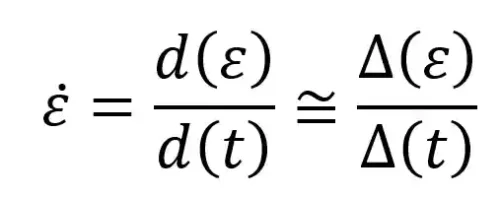
در عمل و در روشهای مبتنی بر داپلر، نرخ استرین را میتوان تقریباً با اختلاف سرعت دو نقطه تقسیم بر فاصله بین آنها نوشت:
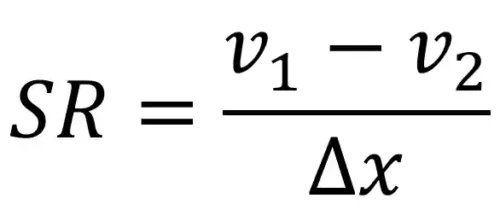
که (v۱) و (v۲) سرعتهای محلی بافت هستند و (x∆) فاصله بین آن دو نقطه است. واحد نرخ استرین معمولاً (s^{-1}) (یک بر ثانیه) است.
⚖️چرا این دو پارامتر مهماند و چه تفاوتی با EF دارند؟
EF (Ejection Fraction؛ درصد تخلیه یا کسر جهشی) یک معیار حجمی است: چه درصدی از حجم بطن در هر ضربان تخلیه میشود. EF تصویر کلی عملکرد پمپاژ را میدهد اما حساسیت محدودی برای تغییرات موضعی یا زودرس دارد. استرین و نرخ استرین به ما میگویند «هر بخش از عضله چگونه و با چه سرعتی حرکت میکند»؛ بنابراین میتوانند اختلالات موضعی یا بالینی را پیش از افت EF نشان دهند.
مثال: اگر یک تیم فوتبال را بطن در نظر بگیریم، EF مثل نتیجه کلی بازی است، اما استرین نشان میدهد هر بازیکن (هر بخش دیواره) چقدر فعال و هماهنگ بازی میکند.
⌛الگوهای زمانی در سیکل قلبی:
- در سیستول (انقباض) استرین طولی معمولاً به مقادیر منفی میرود (مثلاً (-۱۸%) تا (-۲۲%) در افراد سالم).
- نرخ استرین در سیستول نشاندهنده قدرت انقباضی است؛ مقدار کمتر از حد انتظار میتواند نشاندهنده کاهش inotropy (قدرت انقباضی) باشد.
- در دیاستول، نرخ استرین زودهنگام (early diastolic SR) و نرخ استرین مرتبط با پر شدن دهلیزی (late diastolic SR) میتوانند اطلاعاتی درباره شلشدن و ارتجاعپذیری میوکارد بدهند؛ در نمودارها معمولاً دو پیک دیده میشود که با پیکهای E و A در داپلر همزمانی دارند.
👩⚕️مثالهای بالینی ساده :
- بیمار تحت شیمیدرمانی: اگر GLS (مقدار میانگین استرین طولی بطن چپ) از (-۲۰%) به (-۱۶%) تغییر کند، این کاهش نشاندهنده آسیب زودرس است حتی اگر EF هنوز طبیعی باشد؛ این هشدار به پزشک اجازه میدهد درمان محافظتی یا تغییر در رژیم دارویی را در نظر بگیرد.
- ایسکمی موضعی: یک ناحیه از دیواره که استرین بخشبندیشدهاش کمتر از نواحی اطراف است، ممکن است نشاندهنده خونرسانی ناکافی یا اسکار باشد؛ این را میتوان با نقشه رنگی و منحنیهای زمانی بهراحتی دید.
- دیاستولیک: کاهش در نرخ استرین در مراحل اولیه دیاستول(early diastolic) میتواند نشاندهنده سفتی دیواره و اختلال در پر شدن بطن باشد، حتی پیش از تغییرات واضح در فشارها یا EF.
🧩سگمنتیشن در استرین اکو
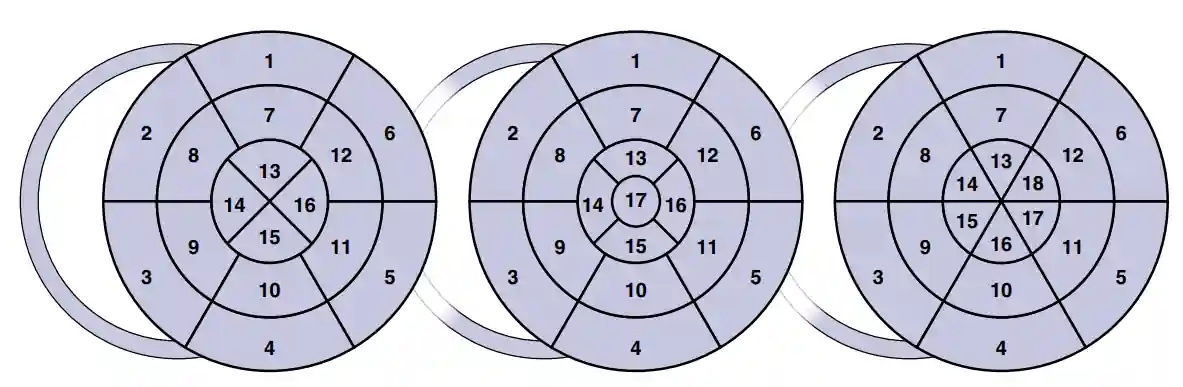
سگمنتیشن در استرین اکو به فرایند تعیین و جدا کردن نواحی (سگمنتها) و مرزهای دیوارهی میوکارد در تصاویر اکو گفته میشود تا ردیابی لکه (speckle tracking) و محاسبه کرنش برای هر بخش بهصورت مجزا انجام شود. این کار شامل مشخصکردن مرز اندوکاردیال و اپیکاردیال و تقسیمبندی دیواره به سگمنتهای استاندارد (مثلاً ۱۶ یا ۱۷ سگمنت) است. (American Society of Echocardiography Number Analytics)
هدف و خروجیها
- هدف اصلی: فراهمکردن نواحی مرجع برای ردیابی الگوهای لکهای و استخراج مقادیر کرنش و جابجایی بهصورت سگمنتال و جهانی. (Number Analytics)
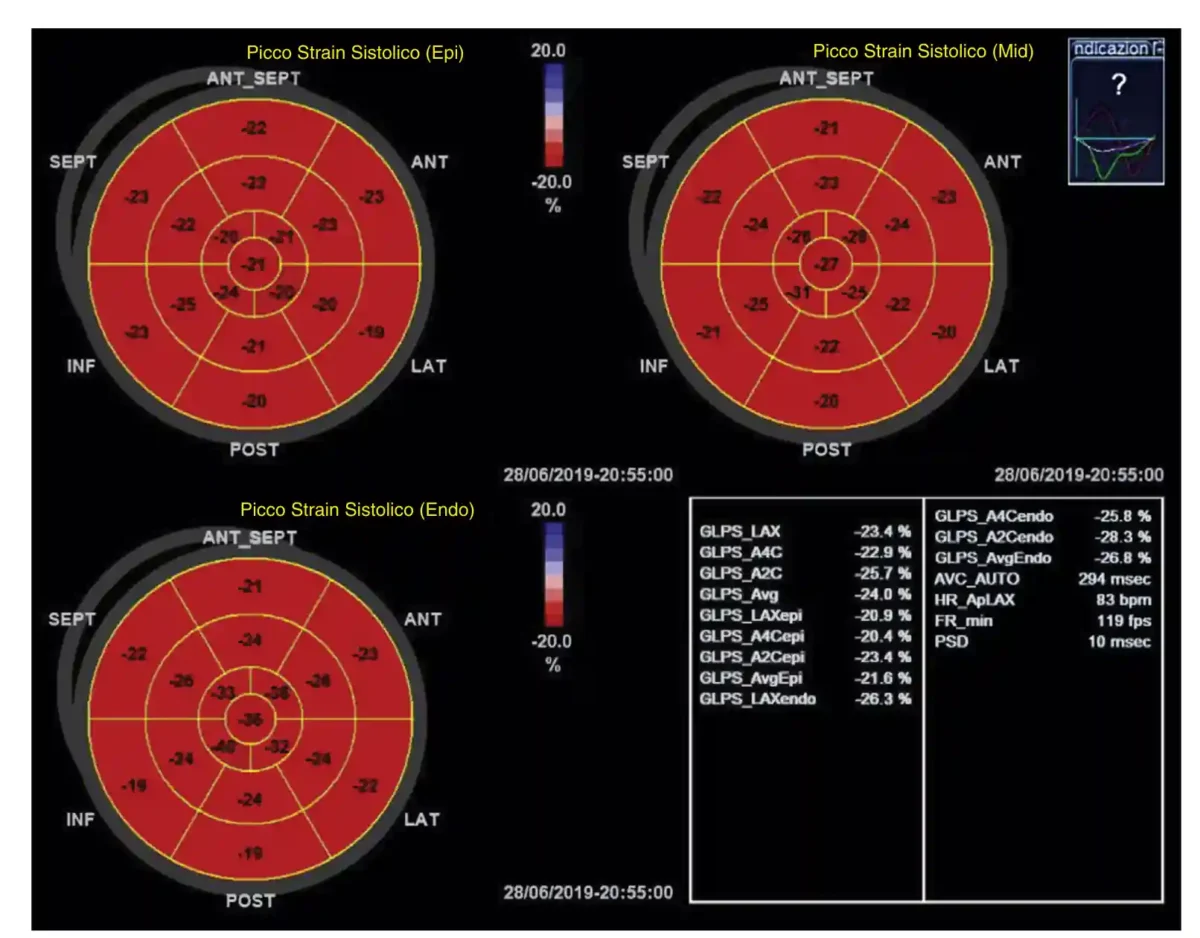
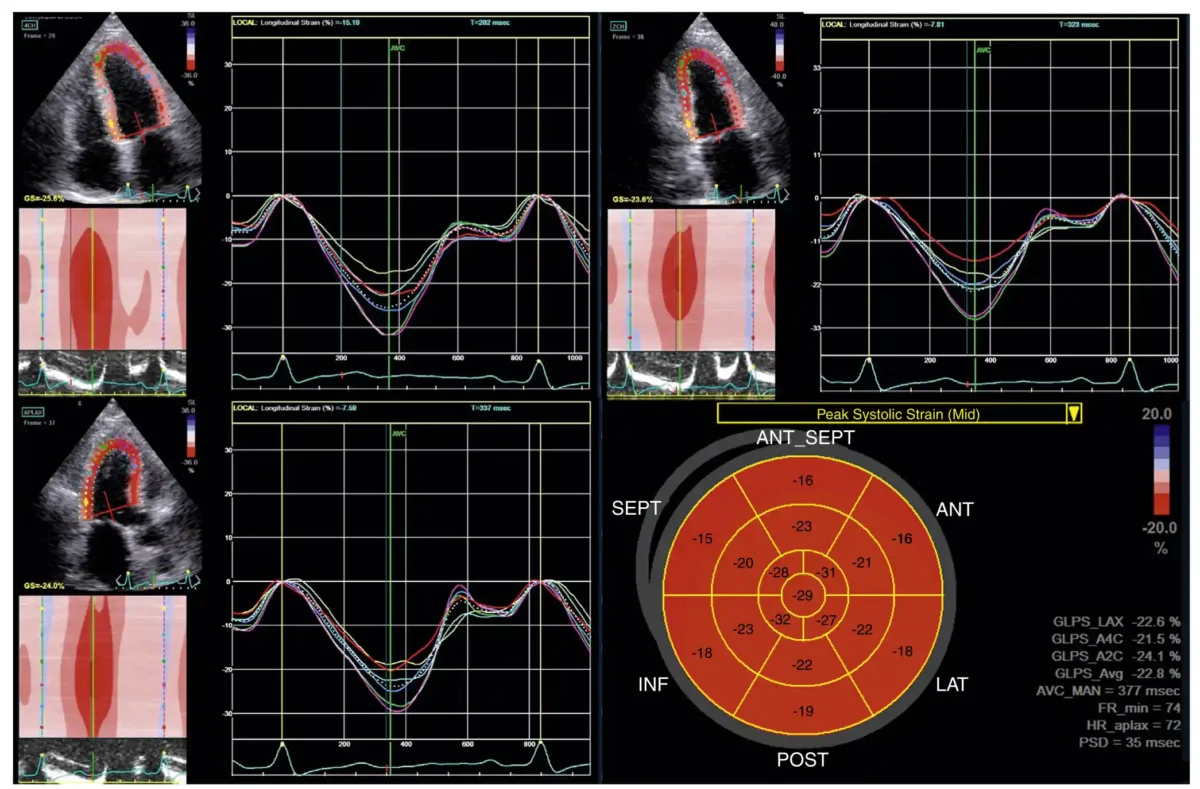
- خروجیهای معمول: منحنیهای زمانی کرنش برای هر سگمنت، نقشه بولزآی (bull’s‑eye) برای نمایش منطقهای کرنش، و مقادیر لایهای (اندوکاردیال/میدوال/اپیکاردیال) در صورت انجام سگمنتیشن چندلایهای. (cdn.intechopen.com)
روشها و سطوح اتوماسیون
- دستی: اپراتور با رسم کانتورهای اندوکارد و اپیکارد بهصورت دستی سگمنتها را تعیین میکند؛ دقیق اما زمانبر و وابسته به اپراتور است.
- نیمهخودکار: نرمافزار کانتور اولیه را پیشنهاد میدهد و اپراتور آن را اصلاح میکند؛ تعادل بین سرعت و دقت.
- خودکار: الگوریتمهای پردازش تصویر یا شبکههای عصبی کانولوشنی کانتور و تقسیمبندی را بهصورت خودکار تولید میکنند؛ سریع اما نیازمند اعتبارسنجی و کنترل کیفیت. (Springer Number Analytics)
اهمیت بالینی و فنی
- قابلیت تکرار و مقایسهپذیری: سگمنتیشن استاندارد (نماها و تقسیمبندی یکسان) امکان مقایسه بین زمانها و بین مراکز را فراهم میکند. American Society of Echocardiography
- دقت محاسبات کرنش: محل دقیق کانتورها و تقسیمبندی تعیینکنندهی مقادیر کرنش سگمنتال و جهانی است؛ خطا در سگمنتیشن میتواند نتایج را بهطور قابلتوجهی تغییر دهد. Number Analytics
محدودیتها و خطاهای رایج
- کیفیت تصویر پایین، فُرشورتینگ (foreshortening)، و حرکت خارج صفحه باعث خطا در تعیین مرزها و ردیابی میشوند.
- تفاوت بینسازندهای و نسخههای نرمافزاری میتواند منجر به اختلاف در سگمنتیشن و مقادیر کرنش شود؛ استانداردسازی و اعتبارسنجی بینمرکزی ضروری است. American Society of Echocardiography
بهترین شیوهها (پیشنهادات عملی)
- ثبت نماهای استاندارد آپیکال (۲‑, ۳‑, ۴‑ch) با فریمریت مناسب و همزمانی ECG.
- استفاده از روش نیمهخودکار با بازبینی اپراتور برای تعادل بین سرعت و دقت.
- گزارشدادن متادیتا (نما، فریمریت، نسخه نرمافزار) و انجام کنترل کیفیت تصویری قبل از تحلیل. Number Analytics cdn.intechopen.com
📐متغیرهای اصلی مبتنی بر استرین
🌟GLS (Global Longitudinal Strain) : میانگین تغییر طول (استرین طولی) تمام سگمنتهای بطن چپ در راستای طولی؛ نشاندهنده میزان کوتاه شدن الیاف طولی در سیستول است. مقادیر نرمال در بزرگسالان سالم معمولاً در حدود −۱۸% تا −۲۲% گزارش میشود. (American Society of Echocardiography Guideline Central)مقدار مطلق کمتر (مثلاً تغییر از −۲۰% به −۱۶%) نشاندهنده کاهش عملکرد طولی و هشدار زودرس برای اختلال میوکارد است؛ در پیگیری بیماران (مثلاً تحت شیمیدرمانی) کاهش قابلتوجه GLS نسبت به پایه میتواند نیاز به مداخله یا تغییر درمان را مطرح کند. GLS حساس و قابلتکرار است اما تحت تأثیر بارگذاری و اختلافات بین سازندگان دستگاه قرار میگیرد؛ بنابراین پیگیریها بهتر است با همان دستگاه/نرمافزار انجام شود. (European Society of Cardiology)
🌟GCS (Global Circumferential Strain) : میانگین استرین دورانی یا عرضی دیواره بطن چپ که نشاندهنده انقباض عرضی و «جمعشدن» حلقوی دیواره است. مقادیر نرمال (تقریبی)معمولاً مقادیر منفی و در محدودهای مشابه یا کمی کمتر از GLS گزارش میشوند (مقادیر مرجع دقیق بسته به روش و دستگاه متفاوت است). کاهش GCS نشاندهنده اختلال در انقباض عرضی است؛ در برخی کاردیومیوپاتیها یا آسیبهای لایهای، GCS ممکن است تغییرات خاصی نشان دهد که مکمل GLS است. بهدلیل تفاوت الگوریتمها، مقادیر مرجع را از گزارش دستگاه یا راهنماهای محلی باید استناد کرد.
🌟GRS (Global Radial Strain) : میانگین استرین شعاعی که ضخیمشدن دیواره در جهت شعاعی (از اپیکارد به اندوکارد) را در سیستول نشان میدهد. مقادیر نرمال (تقریبی) معمولاً مثبت و بزرگتر از مقادیر طولی/عرضی (مثلاً چند ده درصد؛ عدد دقیق وابسته به روش و مرجع). کاهش GRS نشاندهنده کاهش ضخامت انقباضی دیواره؛ در برخی شرایط که تغییرات حجمی یا هندسی رخ میدهد، GRS میتواند اطلاعات تکمیلی بدهد. GRS بهخاطر وابستگی به هندسه و کیفیت تصویر متغیرتر است و در پیگیریها باید با احتیاط تفسیر شود.
🌟Peak Systolic Strain : بیشترین مقدار استرین ثبتشده در فاز سیستول برای یک سگمنت یا برای میانگین کلی (مثلاً GLS peak). مقادیر نرمال تابع نوع استرین (طولی/عرضی/شعاعی) و مرجع است؛ برای طولی معمولاً در محدوده GLS طبیعی قرار میگیرد. کاهش peak systolic strain در یک سگمنت میتواند نشاندهنده ایسکمی موضعی یا اسکار باشد.
🌟Strain Rate (SR) : سرعت تغییر استرین در واحد زمان؛ نشاندهنده «سرعت» انقباض یا بازگشت بافت. واحد آن (s^{-1}) (یک بر ثانیه) است. اجزای مهم SR سیستولیک (سرعت انقباض) و SR دیاستولیک زودهنگام (early diastolic SR؛ سرعت شلشدن/بازگشت). SR سیستولیک بازتابدهنده inotropy (قدرت انقباضی) است و کاهش آن میتواند نشاندهنده کاهش توان انقباضی سلولی باشد؛ SR دیاستولیک اطلاعاتی درباره ارتجاعپذیری و پر شدن بطن میدهد و در تشخیص اختلالات دیاستولیک مفید است. SR کمتر از استرین تحت تأثیر بارگذاری نیست و میتواند اطلاعات تکمیلی درباره عملکرد ذاتی میوکارد بدهد، اما مقادیر مرجع بین روشها متفاوت است.
🌟Segmental (Regional) Strain : استرین محاسبهشده برای هر سگمنت دیواره (معمولاً ۱۶ یا ۱۷ سگمنت استاندارد) است. مقادیر نرمال هر سگمنت باید در محدودههای مرجع مربوط به نوع استرین باشد؛ اختلاف قابلتوجه بین سگمنتها غیرطبیعی است. الگوهای نامتوازن یا کاهش موضعی استرین میتواند نشاندهنده ایسکمی منطقهای، اسکار پس از انفارکتوس یا اختلال عملکرد موضعی ناشی از بیماریهای ساختاری باشد؛ نقشههای رنگی و منحنیهای زمانی کمک میکنند تا زمانبندی و شدت اختلال مشخص شود.
🌟Layer‑specific Strain (استرین لایهای): اندازهگیری استرین جداگانه در لایههای اندوکاردیال، میانی و اپیکاردیال. تغییرات لایهای میتواند الگوی آسیب را نشان دهد (مثلاً اندوکاردیال در ایسکمی بیشتر درگیر میشود). با این حال تحلیل لایهای فنیتر و حساس به کیفیت تصویر است و در برخی راهنماها توصیه میشود با احتیاط و در موارد خاص استفاده شود. (American Society of Echocardiography)
🌟Twist / Torsion (پیچش و تابش): اختلاف چرخش بین قاعده و قله بطن چپ که حرکت پیچشی قلب را نشان میدهد؛ معمولاً به صورت درجه یا درجه بر سانتیمتر گزارش میشود. تغییر در twist/torsion میتواند در کاردیومیوپاتیها، اختلالات هماهنگی و برخی بیماریهای متابولیک دیده شود و اطلاعات تکمیلی درباره ذخیره انرژی مکانیکی قلب فراهم میآورد. اندازهگیری دقیق نیازمند نماهای کوتاهمحور و/یا 3D‑STE و استانداردسازی بین دستگاهها است.
🌟RV Free‑Wall Strain (استرین دیواره آزاد بطن راست) : میانگین استرین طولی دیواره آزاد بطن راست؛ در ارزیابی عملکرد بطن راست کاربرد دارد. مقادیر نرمال (تقریبی) معمولاً مقادیر منفی و در محدودهای مشابه GLS ولی با مرجعهای اختصاصی برای RV. کاهش این مقدار نشاندهنده اختلال عملکرد بطن راست است و در بیماریهای ریوی، فشار شریانی ریوی و نارسایی سمت راست اهمیت دارد.
نکات کلی تفسیر بالینی و محدودیتها: مقادیر مرجع دقیق برای هر متغیر به روش (2D vs 3D)، الگوریتم نرمافزاری و سازنده دستگاه وابسته است؛ بنابراین vendor variability یک محدودیت مهم است و راهنماهای تخصصی توصیه به استانداردسازی و گزارش مرجع دستگاه دارند. (European Society of Cardiology American Society of Echocardiography) همچنین استرین تحت تأثیر شرایط بارگذاری (preload/afterload)، کیفیت تصویر و فریمریت قرار میگیرد؛ تغییرات بالینی باید در زمینه تصویر بالینی بیمار، EF، یافتههای داپلر و آزمایشهای تکمیلی تفسیر شوند.
| متغیر | تعریف کوتاه | واحد / نمایش | تفسیر کلی |
|---|---|---|---|
| GLS (Global Longitudinal Strain) | میانگین استرین طولی کل بطن چپ؛ نشاندهنده کشش طولی میوکارد. | درصد (معمولاً منفی، مثال: −۲۰%) | مقادیر مطلق کمتر (مثلاً از −۲۰% به −۱۶%) نشاندهنده کاهش عملکرد طولی است. |
| GCS (Global Circumferential Strain) | میانگین استرین دورانی/عرضی بطن چپ؛ نشاندهنده انقباض عرضی دیواره. | درصد (معمولاً منفی) | کاهش نشاندهنده اختلال در انقباض عرضی؛ در برخی بیماریها زودتر از EF تغییر میکند. |
| GRS (Global Radial Strain) | میانگین استرین شعاعی؛ ضخیمشدن دیواره در زمان سیستول. | درصد (معمولاً مثبت) | کاهش GRS نشاندهنده کاهش ضخامت انقباضی دیواره است. |
| Peak Systolic Strain | بیشترین مقدار استرین ثبتشده در فاز سیستول برای یک ناحیه یا کل بطن. | درصد | معیار عملی برای سنجش حداکثر انقباض هر بخش. |
| Strain Rate (SR) | سرعت تغییر استرین در واحد زمان؛ نشاندهنده سرعت انقباض یا بازگشت. | (s^{-1}) (یک بر ثانیه) | SR سیستولیک بازتابدهنده inotropy (قدرت انقباضی) است؛ SR دیاستولیک اطلاعاتی درباره شلشدن و پر شدن دارد. |
| Segmental (regional) strain | استرین محاسبهشده برای هر سگمنت دیواره (مثلاً ۱۶ یا ۱۷ سگمنت). | درصد | برای شناسایی نواحی ایسکمیک، اسکار یا دیسکینزی مفید است. |
| Layer‑specific strain | استرین لایهای (اندوکارد، میوکارد میانی، اپیکارد) | درصد | تغییرات لایهای میتواند الگوی آسیب (مثلاً اندوکاردیال در ایسکمی) را نشان دهد. |
| Twist / Torsion | چرخش نسبی قاعده و قله بطن چپ؛ نشاندهنده حرکت پیچشی قلب. | درجه یا درجه/سانتیمتر | تغییر در torsion میتواند در کاردیومیوپاتیها و اختلالات مکانیکی دیده شود. |
📔کلیات تفسیر
تفسیر نتایج استرین باید با مشخصکردن هدف بالینی آغاز شود: آیا اندازهگیری برای تشخیص اولیه، پایش تغییرات در طول زمان، یا پیشآگهی بیمار انجام شده است؟ هدف مشخص میکند کدام پارامترها (مثلاً GLS — کشش طولی کلی) اهمیت بیشتری دارند و چه آستانههایی برای اقدام بالینی قابلاتکا هستند. نتایج استرین همیشه بخشی از یک تصویر بزرگترند؛ ترکیب آنها با EF (درصد تخلیه بطن چپ)، یافتههای داپلر (Doppler؛ روش اندازهگیری جریان خون و سرعت)، علائم بیمار و آزمایشهای خونی مانند تروپونین یا BNP، تفسیر را قابلاطمینانتر میکند. یک عدد تنها به ندرت به تنهایی تصمیمگیرنده است. کیفیت تصویر پایه هر تحلیل است: فریمریت مناسب، مرزهای واضح اندوکاردیال و نبود لرزش یا آرتیفکت حرکتی شرط لازم برای نتایج قابلاعتماد است. اگر نرمافزار ردیابی لکهها (Speckle‑Tracking) نتواند الگوها را بهخوبی دنبال کند، باید در گزارش ذکر شود و تفسیر محافظهکارانه ارائه گردد.
در گزارش حتماً باید مرجع مورد استفاده ذکر شود؛ مقادیر مرجع GLS و سایر پارامترها بسته به سن، جنس و الگوریتم نرمافزاری متفاوت است. نوشتن مرجع به خواننده کمک میکند بداند آیا تغییر مشاهدهشده واقعی است یا ناشی از تفاوت بین دستگاهها. تغییرات کوچک و گذرا را نباید بیش از حد تفسیر کرد. برای مثال در پایش بیماران تحت شیمیدرمانی، کاهش پیوسته و قابلتوجه GLS نسبت به مقدار پایه اهمیت دارد؛ یک نوسان جزئی ممکن است ناشی از تغییرات همودینامیک یا کیفیت تصویر باشد. وضعیت همودینامیک بیمار در زمان اکو باید ثبت شود، زیرا بارگذاری (preload؛ حجم ورودی و afterload؛ مقاومت خروجی) میتواند استرین را تغییر دهد. فشار خون بالا یا کمآبی میتواند بدون تغییر ذاتی در میوکارد، مقادیر استرین را جابهجا کند؛ بنابراین تفسیر باید این شرایط را لحاظ کند.
اختلاف بین سازندگان دستگاهها (vendor variability) یک واقعیت عملی است: الگوریتمها و مقادیر مرجع میتوانند متفاوت باشند، بنابراین پیگیریهای متوالی بهتر است با همان دستگاه و نسخه نرمافزاری انجام شود یا در گزارش تفاوت دستگاهها قید شود تا تغییرات کاذب مشخص بماند. گزارش استاندارد باید فراتر از عدد باشد: علاوه بر مقدار (مثلاً GLS = −۱۹%)، کیفیت ردیابی، نماهای استفادهشده (AP4 — نما آپیکال چهارحفرهای، AP2 — نما آپیکال دوحفرهای، AP3 — نما آپیکال سهحفرهای) و هر اصلاح دستی انجامشده ذکر شود. این اطلاعات به خواننده امکان میدهد اعتماد به نتیجه را بسنجند. برای تصمیمگیری بالینی، مراکز معمولاً الگوریتمهای محلی تدوین میکنند؛ مثلاً در پایش کاردیوکسیکوتوکسیته، کاهش مطلق GLS بیش از مقدار مشخص یا کاهش نسبی نسبت به پایه میتواند علامت لزوم ارزیابی بیشتر یا شروع درمان محافظتی باشد. این الگوریتمها باید با توجه به شواهد و منابع محلی تنظیم شوند.
در نهایت، تفسیر استرین نیازمند آموزش و کنترل کیفیت مستمر: آزمونهای بینناظر (inter‑observer) و درونناظر (intra‑observer)، بازبینی دورهای نتایج و آموزش اپراتورها است که تضمین میکند که این ابزار بهصورت قابلاعتماد در مراقبت از بیماران بهکار رود.
استرین اکو یک ابزار تکمیلی قدرتمند است که در بسیاری از بیماریهای قلبی اطلاعات زودرس و منطقهای میدهد و میتواند تشخیص، تفکیک افتراقی و تصمیمگیری درمانی را تکمیل کند؛ اما در همه موارد مستقل و قطعی نیست و محدودیتهایی مانند تأثیر بارگذاری، کیفیت تصویر و اختلاف الگوریتمی بین سازندگان وجود دارد که باید در تفسیر بالینی لحاظ شوند. Oxford Academic Springer
🩺نقش بالینی استرین اکو
استرین اکو وقتی بیشترین ارزش را دارد که هدف، کشف تغییرات عملکرد مکانیکی میوکارد در سطح میکرو یا منطقهای باشد؛ یعنی زمانی که میخواهیم بفهمیم هر بخش از دیواره قلب چگونه منقبض و شل میشود، نه فقط اینکه حجم کلی پمپاژ چقدر است. در این موقعیتها، مثل پایش قلب بیماران تحت شیمیدرمانی، تشخیص اختلالات زیر بالینی قبل از افت درصد تخلیه (EF؛ Ejection Fraction، درصد تخلیه بطن چپ) یا شناسایی نواحی ایسکمیک موضعی، استرین (strain؛ کرنش یا تغییر شکل) و نرخ استرین (strain rate؛ سرعت تغییر شکل) اطلاعاتی میدهد که روشهای حجمی سنتی قادر به ارائه آن نیستند.
استرین ابزار حساسی برای آشکارسازی «آسیب زودرس» است؛ یعنی زمانی که سلولهای میوکارد هنوز حجم پمپاژ کلی را حفظ کردهاند اما هماهنگی یا قدرت انقباضی موضعی کاهش یافته است. این ویژگی باعث میشود در تصمیمگیریهای پیشگیرانه مفید باشد: مثلاً در بیمارانی که داروهای کاردیوتوکسیک دریافت میکنند، کاهش پیوسته در GLS (Global Longitudinal Strain؛ کشش طولی کلی) میتواند قبل از افت EF هشدار دهد و فرصت مداخله محافظتی فراهم کند.
از سوی دیگر، استرین در شرایطی که تغییرات همودینامیک سریع یا شدید وجود دارد، میتواند گمراهکننده باشد. فشار خون بالا، تغییرات حجم خون (preload؛ بار پیشبارگذاری) یا مقاومت خروجی (afterload؛ پسبارگذاری) میتوانند مقادیر استرین را بدون تغییر ذاتی در بافت میوکارد جابهجا کنند. در این سناریوها تکیه صرف بر استرین ممکن است منجر به تشخیص اشتباه یا اقدامات غیرضروری شود؛ بنابراین همیشه باید وضعیت همودینامیک بیمار همزمان ثبت و در تفسیر لحاظ شود.
در حضور محدودیتهای فنی نیز استرین قابلاعتماد نیست: پنجره آکوستیک ضعیف (poor acoustic window؛ پنجره صوتی نامناسب)، پروتزهای دریچهای که سایه آکوستیک ایجاد میکنند، یا ریتمهای نامنظم مثل فیبریلاسیون دهلیزی باعث میشوند ردیابی لکهها (speckles) ناقص شود و نتایج ناپایدار شوند. در این موارد روشهای جایگزین یا تکمیلی مانند MRI قلبی (Cardiac MRI؛ تصویربرداری رزونانس مغناطیسی قلب) یا اکو ترانسازوفاژیال (TEE؛ اکوی مری) اطلاعات قابلاعتمادتری فراهم میکنند.
استرین همچنین در تشخیصهایی که نیاز به بافتنگاری مستقیم یا دید آناتومیک دقیق دارند، محدود است. برای تفکیک اسکار از التهاب یا تعیین زندهمانی میوکارد، MRI با تأخیر تزریق گادولینیوم (LGE؛ تصویربرداری با تأخیر برای نشاندادن اسکار) استاندارد طلایی است و استرین تنها میتواند کاهش عملکرد را نشان دهد، نه ماهیت بافت را. به همین ترتیب، برای تشخیص تودهها، وِژِتاسیونهای عفونی یا تنگی آناتومیک عروق کرونری، تصویربرداری آناتومیک یا تهاجمی لازم است.
یک محدودیت عملی دیگر، اختلاف الگوریتمی بین سازندگان دستگاهها (vendor variability) و حساسیت به پارامترهای اکتساب است؛ دو دستگاه یا دو نسخه نرمافزاری ممکن است برای یک بیمار مقادیر متفاوتی گزارش کنند. این واقعیت تفسیر روندی را دشوار میسازد مگر اینکه پیگیریها با همان دستگاه/نرمافزار انجام شود یا تغییرات بیندستگاهی تصحیح شوند. بنابراین استرین بهترین عملکرد را زمانی دارد که در یک چارچوب کنترلشده، با کیفیت تصویر مناسب و در ترکیب با سایر دادههای بالینی بهکار رود.
خلاصه اینکه استرین اکو یک حسگر ظریف و قدرتمند برای عملکرد مکانیکی میوکارد است: بسیار مفید وقتی دنبال تغییرات زودرس، منطقهای یا لایهای هستیم؛ اما کمفایده یا حتی منحرفکننده وقتی شرایط همودینامیک متغیر، کیفیت تصویر پایین، ریتم نامنظم یا نیاز به بافتنگاری مستقیم وجود دارد. تفسیر درست مستلزم تلفیق نتایج استرین با EF، داپلر، بیومارکرها و تصویربرداری تکمیلی و توجه دقیق به شرایط فنی و بالینی در زمان اندازهگیری است.
🧩بیماریهایی که استرین اکو تشخیص افتراقی را بهبود میبخشد
✅بیماری ایسکمیک قلبی و انفارکتوس میوکارد (Ischemic heart disease / Myocardial infarction)
در بیمارانی که خونرسانی ناحیهای به میوکارد مختل شده است، استرین سگمنتال (استرین منطقهای) میتواند نواحی با کاهش عملکرد موضعی را زودتر از تغییرات در EF (درصد تخلیه بطن چپ) نشان دهد و الگوی زمانی منحنیهای استرین کمک میکند بین ایسکمی حاد، ناحیهای با اختلال عملکرد گذرا و اسکار مزمن تمایز قائل شویم. در عمل، کاهش موضعی پیوسته در peak systolic strain یا عدم بازگشت مناسب در دیاستول میتواند نشاندهنده اسکار یا ناحیهای با خونرسانی ناکافی باشد؛ با این حال برای افتراق قطعی اسکار از ایسکمی نیاز به تصویربرداری تکمیلی (مثلاً MRI با تأخیر تزریق — LGE) یا آنژیوگرافی است. Oxford Academic
- زمان اندازهگیری: در بیمارانی که درد قفسه سینه دارند یا سابقه آنژین/آنژیوگرافی مثبت؛ بلافاصله پس از بازپرfusion (مثلاً آنژیوپلاستی) و در پیگیریهای بعدی برای ارزیابی بازگشت عملکرد.
- آستانههای هشداردهنده: کاهش موضعی قابلتوجه در peak systolic strain یک یا چند سگمنت نسبت به سگمنتهای مجاور؛ کاهش کلی GLS نسبت به مرجع یا نسبت به پایه میتواند نشاندهنده اختلال منتشر یا چندنقطهای باشد (مرجع کلی GLS حدود −۱۸% تا −۲۲%).
- اقدامات بالینی: کاهش موضعی پایدار → بررسی تکمیلی با MRI با تأخیر تزریق (LGE) یا آنژیوگرافی؛ کاهش گسترده GLS یا افت روندی → ارزیابی برای نارسایی حاد، درمان دارویی حمایتی و پیگیری کوتاهمدت؛ استفاده از استرین برای تفکیک ایسکمی گذرا (stunning) از اسکار مزمن در کنار بالینی و تصویربرداری تکمیلی.
✅نارسایی قلبی با EF کاهشیافته (HFrEF؛ Heart failure with reduced EF)
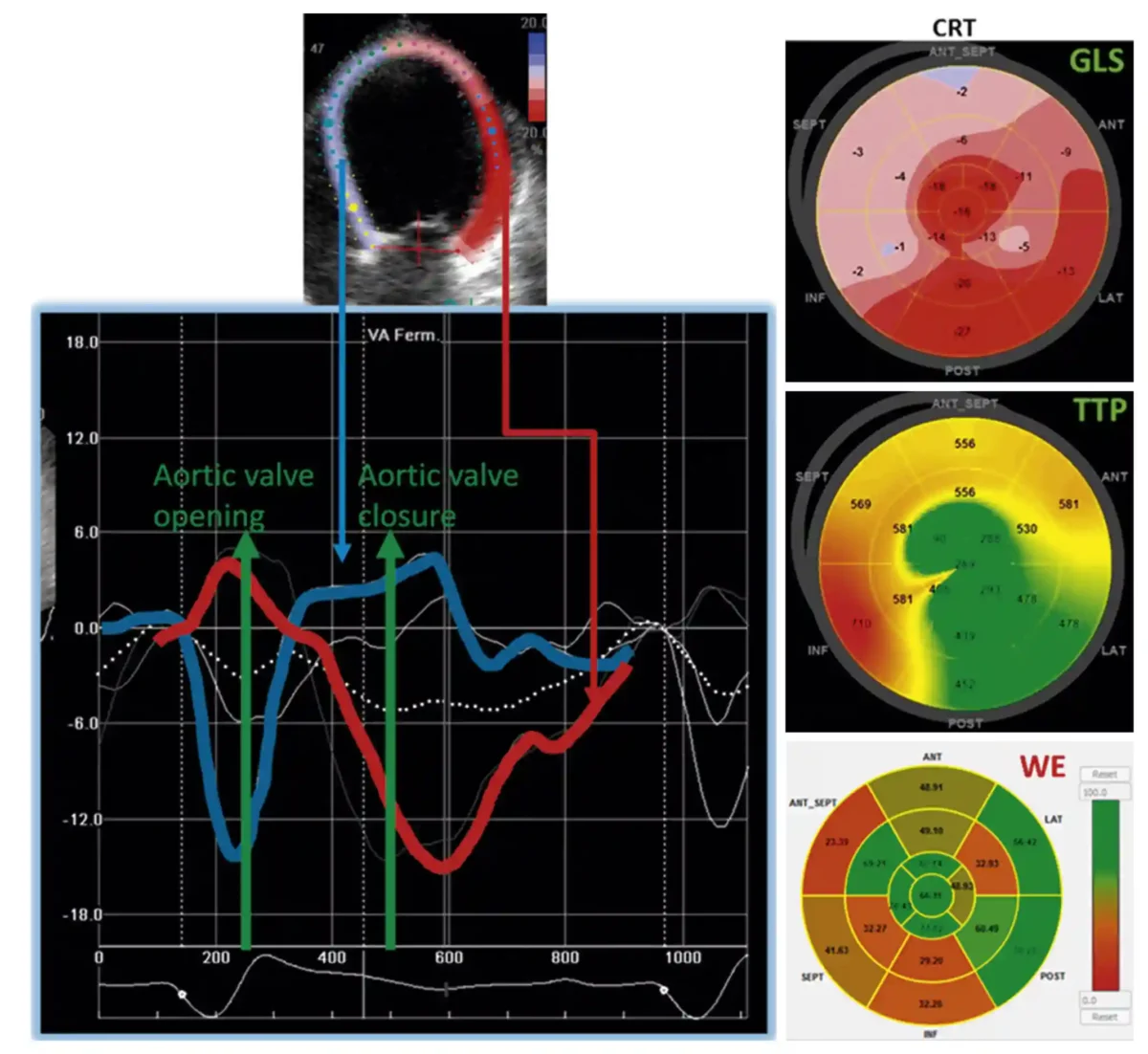
در بیمارانی که EF کاهش یافته است، استرین (بهویژه GLS — کشش طولی کلی) اطلاعات تکمیلی درباره شدت اختلال مکانیکی و هماهنگی دیوارهها میدهد و میتواند در پیشبینی پاسخ به درمانهای دارویی یا دستگاهی (مثلاً CRT — تحریک همزمان بطنها) مفید باشد. استرین در این گروه معمولاً همراستا با EF تغییر میکند اما گاهی الگوهای لایهای یا عدمهماهنگی زمانی که با استرین آشکار میشوند، به انتخاب درمانهای هدفمند کمک میکنند. Springer
- زمان اندازهگیری : در تشخیص اولیه نارسایی، قبل از شروع یا تغییر درمانهای قلبی-دارویی و در ارزیابی پاسخ به درمانهای دارویی یا دستگاهی (مثلاً CRT — تحریک همزمان بطنها).
- آستانههای هشداردهنده: GLS بسیار کاهشیافته (مثلاً کمتر از −۱۲% تا −۱۴% بسته به مرجع) همراه با EF پایین؛ عدمهماهنگی زمانی بین سگمنتها یا کاهش twist/torsion.
- اقدامات بالینی: استرین بهعنوان شاخص تکمیلی برای تعیین شدت اختلال مکانیکی و پیشبینی پاسخ به CRT؛ در صورت عدمهماهنگی یا الگوی خاص، ارجاع برای ارزیابی دستگاهی یا تصویربرداری پیشرفته؛ پایش دورهای برای ارزیابی پاسخ درمانی.
✅نارسایی قلبی با EF طبیعی (HFpEF؛ Heart failure with preserved EF)
در این گروه که EF معمولاً طبیعی است، GLS و پارامترهای دیاستولیک مرتبط با نرخ استرین (early diastolic SR) میتوانند اختلالات عملکردی را نشان دهند که با معیارهای حجمی قابلتشخیص نیستند. کاهش در early diastolic SR یا الگوهای غیرطبیعی لایهای میتواند نشاندهنده سفتی میوکارد و اختلال در ریلکساسیون باشد و به تشخیص HFpEF کمک کند؛ با این حال تفسیر باید با توجه به بارگذاری و بیماریهای همراه انجام شود. Springer
- زمان اندازهگیری: در بیمارانی با علائم نارسایی (تنگی نفس، خستگی) و EF طبیعی؛ زمانی که اختلال دیاستولیک مشکوک است یا بیومارکرها (BNP) بالا هستند.
- آستانههای هشداردهنده: کاهش early diastolic strain rate یا کاهش نسبی GLS در حالی که EF طبیعی است؛ الگوهای لایهای نشاندهنده سفتی میوکارد.
- اقدامات بالینی: تفسیر همراه با داپلر دیاستولیک و بیومارکرها؛ در صورت شواهد اختلال دیاستولیک، مدیریت فشار خون، کنترل حجم و ارزیابی عوامل زمینهای (دیابت، چاقی)؛ استفاده از استرین برای پیگیری پاسخ به درمانهای غیردارویی و دارویی.
✅کاردیوکسیکوتوکسیته ناشی از شیمیدرمانی (Chemotherapy‑related cardiotoxicity)
یکی از کاربردهای بالینی برجسته استرین، پایش بیماران تحت داروهای کاردیوتوکسیک (مثلاً برخی داروهای شیمیدرمانی) است؛ کاهش قابلتوجه GLS اغلب قبل از افت EF رخ میدهد و بهعنوان هشدار اولیه برای مداخله محافظتی یا تغییر رژیم درمانی بهکار میرود. بنابراین استرین در این سناریو بسیار مؤثر است و در پروتکلهای پایش قلبی-عروقی بیماران سرطانی توصیه شده است. Oxford Academic Springer
- زمان اندازهگیری: قبل از شروع داروی کاردیوتوکسیک (baseline)، سپس در فواصل منظم حین درمان (مثلاً هر چرخه یا هر چند هفته بر اساس پروتکل) و پس از اتمام درمان.
- آستانههای هشداردهنده: کاهش مطلق GLS ≥ ۳–۵ درصد نسبت به پایه یا کاهش نسبی ≥ ۱۰–۱۵% بسته به پروتکل؛ افت SR سیستولیک یا تغییرات مداوم در منحنیها.
- اقدامات بالینی: کاهش هشداردهنده → مشاوره کاردیولوژی، بررسی تروپونین/BNP، در نظر گرفتن داروهای محافظتکننده قلب (مثلاً بتابلوکر یا ACE‑I) و تغییر یا توقف داروی توکسیک در هماهنگی با انکولوژیست؛ پیگیری نزدیک با استرین و EF.
✅کاردیومیوپاتی هیپرتروفیک (HCM؛ Hypertrophic cardiomyopathy)
در این بیماری، الگوی استرین میتواند نواحی با اختلال عملکرد لایهای یا عدمهماهنگی را نشان دهد؛ کاهش استرین اندوکاردیال نسبت به اپیکاردیال یا کاهش موضعی در نواحی هیپرتروفیک میتواند به تشخیص و ارزیابی شدت کمک کند. استرین در افتراق HCM از پاتولوژیهای ناشی از بارگذاری (مثلاً هایپرتروفی ناشی از فشار خون) و در پیشبینی ریسک آریتمی یا پیشرفت بیماری مفید است، اما تفسیر نیازمند تجربه و ترکیب با تصویر بالینی و MRI است. Springer
- زمان اندازهگیری: در بیماران با هایپرتروفی دیواره، در خانوادههای در معرض خطر و برای پایش پیشرفت یا ریسک آریتمی.
- آستانههای هشداردهنده: کاهش موضعی استرین در نواحی هیپرتروفیک، کاهش اندوکاردیال نسبت به اپیکاردیال (الگوی لایهای) و کاهش GLS نسبت به مرجع.
- اقدامات بالینی: الگوهای غیرطبیعی → ارزیابی بیشتر با MRI، بررسی ریسک آریتمی و در صورت لزوم مانیتورینگ ریتم یا مداخلات پیشگیرانه؛ استفاده از استرین برای پیگیری تغییرات عملکردی و تصمیمگیری درباره ورزش یا درمانهای تهاجمی.
✅کاردیومیوپاتی دایلته (DCM؛ Dilated cardiomyopathy)
در کاردیومیوپاتی دایلته، کاهش گسترده در GLS و تغییرات در twist/torsion (پیچش قلب) نشاندهنده اختلال مکانیکی منتشر است. استرین میتواند در تفکیک بین اختلال عملکرد اولیه میوکارد و تغییرات ثانویه به بارگذاری کمک کند و در پایش پاسخ به درمانهای دارویی یا پیوند/دستگاههای کمکی قلبی اطلاعات ارزشمندی بدهد؛ با این حال در موارد با تغییرات هندسی شدید یا کیفیت تصویر پایین، دقت کاهش مییابد. Springer
- زمان اندازهگیری: در تشخیص اولیه، قبل از شروع درمانهای قلبی و در پیگیری پاسخ به درمان دارویی یا دستگاهی.
- آستانههای هشداردهنده: کاهش گسترده GLS (معمولاً بسیار کمتر از مرجع)، کاهش twist/torsion و عدمهماهنگی زمانی بین سگمنتها.
- اقدامات بالینی: استرین برای ارزیابی شدت اختلال مکانیکی و پیشبینی پاسخ به درمان؛ در صورت کاهش شدید یا عدم بهبود → ارزیابی برای پیوند یا دستگاههای کمکی؛ پیگیری منظم برای تنظیم درمان.
✅میوکاردیت (Myocarditis؛ التهاب میوکارد)
استرین میتواند نواحی با اختلال عملکرد موضعی را نشان دهد و در پیگیری بهبود یا پیشرفت التهاب مفید باشد؛ کاهش موضعی استرین و الگوهای لایهای (مثلاً درگیری اندوکارد یا میوکارد میانی) میتواند با یافتههای MRI و بیومارکرها همراستا باشد. با این حال تشخیص قطعی میوکاردیت اغلب نیازمند ترکیب با MRI، تروپونین و در موارد خاص بیوپسی است، بنابراین استرین یک ابزار تکمیلی قوی اما نه تنها معیار تشخیصی است. Oxford Academic Springer
- زمان اندازهگیری: در بیمارانی با درد قفسه سینه، افزایش تروپونین یا علائم التهابی قلبی؛ در پیگیری بهبود پس از تشخیص.
- آستانههای هشداردهنده: کاهش موضعی یا چندمنطقهای استرین، الگوهای لایهای غیرطبیعی (مثلاً درگیری میانی) و کاهش SR دیاستولیک.
- اقدامات بالینی: یافتههای غیرطبیعی → ترکیب با MRI (برای تشخیص التهابی و اسکار) و بیومارکرها؛ در صورت شواهد عملکردی ضعیف، مدیریت حمایتی و پیگیری برای بهبود یا پیشرفت به کاردیومیوپاتی مزمن.
✅بیماریهای دریچهای (مثلاً تنگی آئورت — Aortic stenosis، نارسایی میترال — Mitral regurgitation)
در بیماریهای دریچهای، استرین میتواند عملکرد بطن را پیش از تغییرات واضح در EF نشان دهد و در زمانبندی مداخله (مثلاً جراحی یا ترمیم دریچه) کمک کند. برای مثال در تنگی آئورت، کاهش GLS ممکن است نشاندهنده شروع اختلال عملکرد میوکارد باشد حتی اگر EF طبیعی بماند؛ با این حال بارگذاری شدید و تغییرات همودینامیک ناشی از خود بیماری دریچهای میتواند مقادیر استرین را تحتتأثیر قرار دهد و تفسیر باید با احتیاط انجام شود. The Anatolian Journal of Cardiology Oxford Academic
- زمان اندازهگیری: پیش از تصمیمگیری برای مداخله (جراحی یا ترانسکاتتر)، در پیگیری بیماران با بیماری متوسط تا شدید و پس از مداخله برای ارزیابی بازگشت عملکرد.
- آستانههای هشداردهنده: کاهش GLS در حالی که EF هنوز طبیعی است (نشانه شروع اختلال میوکارد)؛ در تنگی آئورت، کاهش GLS میتواند نشاندهنده نیاز به مداخله زودتر باشد.
- اقدامات بالینی: کاهش GLS یا تغییرات روندی → ارزیابی جامع همودینامیک، در نظر گرفتن مداخله زودتر و پیگیری پس از ترمیم/تعویض؛ تفسیر باید با توجه به بارگذاری شدید ناشی از بیماری دریچهای انجام شود.
✅فشار شریانی ریوی و اختلال عملکرد بطن راست (Pulmonary hypertension / RV dysfunction)
استرین دیواره آزاد بطن راست (RV free‑wall strain) ابزاری حساس برای ارزیابی عملکرد بطن راست است و در بیماریهایی مانند فشار شریانی ریوی یا نارسایی سمت راست ناشی از بیماری ریوی کاربرد دارد. کاهش این پارامتر میتواند زودتر از معیارهای سنتی نشاندهنده اختلال عملکرد RV باشد و در تصمیمگیری درمانی و پیشآگهی مفید است؛ محدودیتها شامل دشواری اکتساب نماهای مناسب و حساسیت به کیفیت تصویر است. Oxford Academic
- زمان اندازهگیری: در بیمارانی با شک به فشار شریانی ریوی، تنگی نفس نامشخص یا بیماری ریوی مزمن؛ در پیگیری درمان فشار شریانی ریوی.
- آستانههای هشداردهنده: کاهش RV free‑wall strain (استرین دیواره آزاد بطن راست) نسبت به مرجع اختصاصی RV؛ افت عملکرد RV حتی در حضور EF بطن چپ طبیعی.
- اقدامات بالینی: کاهش RV strain → ارزیابی همزمان با اکو داپلر برای فشار شریان ریوی، در نظر گرفتن تستهای تکمیلی (CT، RHC — کاتتریزاسیون راست قلب) و تنظیم درمان ضد فشار شریانی ریوی؛ پیگیری برای پیشبینی بدتر شدن سمت راست.
✅آریتمیوژنیک کاردیومیوپاتی بطن راست و بیماریهای ارثی
در برخی بیماریهای ارثی که منجر به اختلال عملکرد منطقهای میشوند، استرین سگمنتال میتواند نواحی با عملکرد ضعیف یا دیسکینزی را شناسایی کند و در پایش خانوادهها یا تشخیص زودرس مفید باشد. با این حال در تشخیص نهایی و تعیین ریسک آریتمی معمولاً نیاز به ترکیب با MRI، ژنتیک و ارزیابی الکتروفیزیولوژیک وجود دارد. Springer
- زمان اندازهگیری: در خانوادههای در معرض خطر، بیماران با سابقه سنکوپ یا آریتمی، و در پیگیری ژنتیکی.
- آستانههای هشداردهنده: کاهش موضعی یا عدمهماهنگی در استرین سگمنتال RV یا LV؛ الگوهای منطقهای که با اسکار یا جایگزینی چربی/فیبروز همخوانی دارد.
- اقدامات بالینی: یافتههای مشکوک → ارزیابی با MRI، مشاوره ژنتیک و ارزیابی الکتروفیزیولوژیک برای تعیین ریسک آریتمی و نیاز به ایمپلنت دستگاه ضدآریتمی.
✅بیماریهای مادرزادی و پس از جراحی قلب
در بیماران با آناتومی غیرطبیعی یا پس از جراحیهای بازسازی، استرین میتواند عملکرد بخشهای مختلف بطن را بهصورت کمّی دنبال کند و به ارزیابی موفقیت مداخله یا نیاز به اصلاحات بعدی کمک کند. محدودیت اصلی در این گروه، پیچیدگی هندسه و تغییرات آناتومیک است که ممکن است تحلیل خودکار را دشوار کند و نیاز به بررسی دقیق اپراتور و گاهی روشهای سهبعدی (3D‑STE) یا MRI دارد. Springer
- زمان اندازهگیری: قبل و بعد از جراحی یا مداخلات بازسازی، در پیگیری طولانیمدت عملکرد بطنها و در بیماران با آناتومی غیرطبیعی.
- آستانههای هشداردهنده: کاهش عملکرد موضعی یا کلی که با علائم یا تغییرات همودینامیک همراه است؛ تغییرات ناگهانی پس از مداخله.
- اقدامات بالینی: استرین برای ارزیابی موفقیت مداخله و شناسایی نیاز به اصلاحات بعدی؛ در موارد هندسه پیچیده، استفاده از 3D‑STE یا MRI برای تحلیل دقیقتر و تفسیر توسط تیم چندتخصصی.
⚠️بیماریهایی که استرین اکو در تشخیص افتراقی آنها تاثیر کمی دارد
❌پریکاردیت محدودکننده (Constrictive pericarditis؛ التهاب و فیبروز پرده قلب که باعث محدودیت مکانیکی میشود)
استرین اکو در پریکاردیت محدودکننده اطلاعات مکانیکی کلی میدهد اما تشخیص قطعی و تمایز آن از دیستولیک میوکاردیال اغلب نیازمند روشهای دیگر است. علت این است که در پریکاردیت، مشکل اصلی مکانیکی ناشی از پرده (پریکارد) است نه تغییرات ذاتی در بافت میوکارد؛ بنابراین الگوهای استرین ممکن است غیر اختصاصی یا مخلوط باشند. تصویربرداری ساختاری مانند CT (توموگرافی کامپیوتری؛ تصویربرداری مقطعی) یا MRI (تصویربرداری رزونانس مغناطیسی؛ تصویربرداری با میدان مغناطیسی) برای نشاندادن ضخامت، کالسیفیکاسیون و محدودیت پرده و برای تصمیمگیری درمانی (مثلاً پریکاردکتومی) ضروریتر است.
❌تامپوناد قلبی (Cardiac tamponade؛ تجمع مایع فشردهکننده در کیسه پریکاردیال)
در تامپوناد، تغییرات همودینامیک سریع و فشارگذاری (afterload/preload) غالب است و استرین نمیتواند بهسرعت یا اختصاصی علت را نشان دهد. تشخیص و فوریت درمانی بر پایه شواهد بالینی و اکوکاردیوگرافی دو بعدی ساده و داپلر برای مشاهده مایع پریکاردیال و نشانههای فشار بر بطنها است؛ در این وضعیت، اندازهگیری استرین کمکی اندک دارد و ممکن است به دلیل تغییرات بارگذاری شدید گمراهکننده باشد.
❌ تودهها و اندوکاردیت عفونی (Cardiac masses / Infective endocarditis؛ تومورهای داخل قلب یا رشدهای عفونی روی دریچهها)
استرین برای ارزیابی عملکرد میوکارد مفید است اما در تشخیص تودهها، ندولها یا وِژِتاسیونهای عفونی (vegetations) کاربردی ندارد؛ این ساختارهای آناتومیک نیاز به تصویربرداری با رزولوشن بالا و نماهای خاص دارند. تشخیص و ارزیابی اندوکاردیت معمولاً با اکوکاردیوگرافی ترانسازوفاژیال (TEE؛ اکوی مری) و کشت خون انجام میشود؛ استرین نمیتواند جایگزین دید مستقیم و نمونهبرداری یا ارزیابی آناتومی شود.
❌دریچههای مصنوعی و سایهگذاری آکوستیک (Prosthetic valves / Acoustic shadowing؛ دریچههای مصنوعی که مانع دید میشوند)
وجود پروتزهای فلزی یا ساختارهای بزرگ باعث ایجاد سایه آکوستیک (acoustic shadow) میشود که ردیابی لکهها (speckles) را مختل میکند و در نتیجه مقادیر استرین قابلاعتماد نخواهند بود. در این بیماران، روشهای تصویربرداری تکمیلی مانند CT یا MRI و اکوکاردیوگرافی ترانسازوفاژیال برای ارزیابی عملکرد دریچه و نشت (regurgitation) مناسبترند.
❌ریتمهای نامنظم شدید (مثل فیبریلاسیون دهلیزی؛ Atrial fibrillation)
در حضور ریتم نامنظم، تغییرات ضربانی به ضربان (beat‑to‑beat variability) باعث ناپایداری منحنیهای استرین و نرخ استرین میشود و محاسبه میانگین قابلاعتماد دشوار است. اگرچه تکنیکهایی برای میانگینگیری وجود دارد، اما در بسیاری از موارد برای ارزیابی دقیق عملکرد باید ریتم تثبیت شود یا از روشهای تکمیلی استفاده گردد؛ بنابراین در ریتمهای نامنظم، استرین کمتر قابلاعتماد است.
❌ آناتومی مادرزادی پیچیده و قلبهای بازسازیشده (Complex congenital heart disease)
در آناتومیهای غیرطبیعی یا پس از جراحیهای بازسازی، هندسه بطنها تغییر یافته و مرزهای آناتومیک استاندارد برای تقسیمبندی سگمنتال قابلاعمال نیست. الگوریتمهای استرین که برای قلبهای با هندسه طبیعی طراحی شدهاند ممکن است نتایج گمراهکننده تولید کنند؛ در این موارد MRI قلبی یا اکو سهبعدی (3D‑echocardiography) و ارزیابی تخصصی آناتومی ترجیح داده میشود.
❌ ارزیابی قطعی زندهمانی میوکارد (Myocardial viability / scar assessment)
برای تعیین زندهمانی (viability) و تفکیک اسکار از بافت زنده، MRI با تأخیر تزریق گادولینیوم (LGE؛ تصویربرداری با تأخیر برای نشاندادن اسکار) استاندارد طلایی است. استرین میتواند کاهش عملکرد موضعی را نشان دهد اما قادر به تشخیص مستقیم فیبروز یا اسکار با دقت MRI نیست؛ بنابراین وقتی تصمیمگیری درمانی (مثلاً بازتوانی عروق یا پیوند) نیاز به تعیین زندهمانی دارد، MRI ارجح است.
❌بیماریهای عروقی کرونر آناتومیک (آنژیوگرافی نیازمند تشخیص آناتومی؛ Coronary artery stenosis assessment)
اگر هدف تعیین محل و شدت تنگی عروق کرونری باشد، استرین تنها نشاندهنده اثر عملکردی (اختلال موضعی) است و نمیتواند جایگزین آنژیوگرافی (invasive coronary angiography؛ آنژیوگرافی تهاجمی) یا CT آنژیوگرافی برای دیدن آناتومی عروق شود. برای برنامهریزی مداخلات کرونری، تصویربرداری آناتومیک ضروری است.
❌ بیماریهای میکروواسکولار کرونر (Coronary microvascular dysfunction؛ اختلال در ریزعروق)
در میکروواسکولار، بیمار ممکن است درد ایسکمیک داشته باشد بدون تنگی قابلمشاهده در عروق بزرگ؛ استرین ممکن است غیرطبیعی باشد اما غیر اختصاصی و ناتوان از تعیین علت میکروواسکولار است. تشخیص میکروواسکولار معمولاً نیازمند تستهای عملکردی عروق (مثل تستهای استرس با PET یا invasive coronary flow reserve) است که اطلاعات فیزیولوژیک دقیقتری میدهند.
❌ بیماران با پنوموتوراکس یا شرایطی که پنجره آکوستیک را میبندد (Poor acoustic window)
در مواردی که پنجره آکوستیک مناسب وجود ندارد—مثلاً بهخاطر چاقی شدید، بیماریهای ریوی مزمن یا پنوموتوراکس—کیفیت تصویر برای ردیابی لکهها کافی نیست و مقادیر استرین قابلاعتماد نخواهند بود. در این شرایط باید از روشهای تصویربرداری جایگزین مانند MRI یا CT استفاده شود.
استرین اکو ابزار قدرتمندی برای ارزیابی عملکرد مکانیکی میوکارد است اما در شرایطی که نیاز به تشخیص آناتومیک دقیق، بافتشناسی (تعیین اسکار یا التهاب)، دید مستقیم ساختارها (تودهها، وِژِتاسیونها)، یا در حضور موانع فنی (پروتزها، پنجره آکوستیک ضعیف، ریتم نامنظم) وجود دارد، روشهای دیگر (TEE، آنژیوگرافی، CT، MRI، تستهای فیزیولوژیک عروقی) ارجحاند. دلیل اصلی محدودیتها شامل وابستگی به کیفیت تصویر، تأثیر بارگذاری (preload/afterload)، عدم توانایی در بافتنگاری مستقیم و اختلاف الگوریتمی بین دستگاهها است.
🔀الگوریتم های استرین اکو
الگوریتمهای استرین اکو را میتوان بر اساس سه معیار اصلی دستهبندی کرد: نوع ورودی (B‑mode دوبعدی، حجم سهبعدی، یا سیگنال داپلر)، روش استخراج حرکت (ردیابی الگو، محاسبه جریان نوری، برازش مدل فیزیکی یا یادگیری از داده) و خروجی مورد انتظار (سرعت، جابجایی، کرنش یا پارامترهای مکانیکی). این تقسیمبندی کمک میکند تا انتخاب روش متناسب با هدف بالینی (مثلاً اندازهگیری GLS، تشخیص اختلال منطقهای یا استخراج پارامترهای مکانیکی) و محدودیتهای اکتسابی (کیفیت پنجره آکوستیک، فریمریت، وجود ECG) انجام شود. (American Society of Echocardiography)
| گروه | ورودی اصلی | خروجی معمولی | مزیت کلیدی | محدودیت اصلی |
|---|---|---|---|---|
| Speckle Tracking (2D / 3D) | تصاویر B‑mode دوبعدی یا حجمی | میدان جابجایی محلی؛ کرنش سگمنتال و جهانی | مستقل از زاویه؛ حساس به تغییرات منطقهای عملکرد | حساس به کیفیت تصویر و حرکت خارج صفحه |
| Tissue Doppler Imaging TDI | سیگنال داپلر با جهتگیری پرتو | سرعت محلی در جهت محور پرتو؛ مشتق → نرخ کرنش | حساس و با رزولوشن زمانی بالا | وابسته به زاویه؛ فقط مؤلفه محوری را میدهد |
| Block Matching / Optical Flow | جفت فریمهای متوالی B‑mode | میدان سرعت پیکسلی یا بلوکی | پیوستگی فضایی؛ مناسب حرکتهای کوچک و محلی | نویزپذیری؛ نیاز به تنظیم پارامترها |
| Model Based و Physics Informed | میدان جابجایی یا کرنش + مدل مکانیکی | پارامترهای مکانیکی؛ میدان بازسازیشده | استخراج پارامترهای بیوفیزیکی و شبیهسازی پاسخ | نیاز به مدلسازی دقیق و محاسبات سنگین |
| روشهای دادهمحور و یادگیری عمیق | تصاویر خام یا جفت فریم + برچسبها | تخمین مستقیم کرنش یا میدان حرکت | یادگیری الگوهای پیچیده؛ انتها‑به‑انتها | نیاز به داده برچسبخورده زیاد؛ تفسیرپذیری کمتر |
ویژگیهای عملی هر گروه
- Speckle Tracking: بر پایه دنبالکردن الگوهای لکهای در تصاویر B‑mode است و در نسخههای 2D برای نماهای استاندارد و در 3D برای دادههای حجمی بهکار میرود؛ مزیت اصلی، توانایی اندازهگیری کرنش در جهتهای مختلف بدون وابستگی زاویهای مستقیم است، اما دقت آن به پایداری الگوها و کیفیت تصویر وابسته است. این روش در کاربردهای بالینی برای ارزیابی عملکرد منطقهای و محاسبه پارامترهایی مانند GLS پذیرفته شده است. Springer Guideline Central
- Tissue Doppler Imaging: سرعت بافت را در امتداد محور پرتو اندازهگیری میکند و بهخاطر رزولوشن زمانی بالا برای تحلیلهای فازی و نرخهای سریع مفید است؛ با این حال تنها مؤلفه محوری را میدهد و به زاویه بین جهت حرکت و پرتو حساس است، بنابراین در برخی نماها محدودیت دارد. Springer
- Block Matching و Optical Flow: این روشها میدان حرکت را با مقایسه محلی بلوکها یا حل معادلات جریان نوری برآورد میکنند. Block Matching ساده و قابلفهم است و Optical Flow میدان پیوستهتری میدهد؛ هر دو برای حرکتهای کوچک و پیوسته مناسباند اما به نویز و پارامترهای پیادهسازی حساساند و معمولاً نیاز به منظمسازی فضایی‑زمانی دارند. Springer
روشهای مبتنی بر مدل و یادگیری عمیق
- مدلهای فیزیکی و پارامتریک تلاش میکنند با وارد کردن قوانین مکانیکی رفتار میوکارد را توصیف کنند و پارامترهایی مانند سختی یا ویسکوزیته را از دادهها برازش دهند؛ این رویکرد برای استخراج بیومارکرهای مکانیکی و شبیهسازی پاسخ به بارگذاری مناسب است اما نیازمند دادههای با کیفیت و محاسبات عددی پیچیده است.
- یادگیری عمیق (CNNها و شبکههای Optical Flow‑محور) قادر به یادگیری مستقیم نگاشت تصویر→کرنش یا تصویر→میدان حرکت است؛ این روشها در صورت وجود مجموعههای برچسبخورده بزرگ عملکرد بسیار خوبی نشان میدهند ولی تفسیرپذیری کمتری دارند و به استانداردسازی داده و اعتبارسنجی گسترده نیازمندند. ترکیب یادگیری دادهمحور با قیود فیزیکی (physics‑informed) میتواند تعادل بین دقت و فیزیکپذیری را بهبود دهد. (MDPI Springer)
انتخاب الگوریتم مناسب باید بر اساس هدف بالینی، کیفیت و نوع داده، نیاز به تفسیرپذیری و منابع محاسباتی انجام شود. برای پیگیری روندی بیمار یا مطالعات چندمرکزی، ثبات بین‑دستگاهی و گزارش متادیتا (نماها، فریمریت، نسخه نرمافزاری) اهمیت دارد زیرا اختلاف پیادهسازیها میتواند نتایج کمی متفاوت تولید کند. اعتبارسنجی با فانتوم یا مرجعهای تصویربرداری (مثلاً MRI‑tagging) و گزارش معیارهای خطا (RMSE/MAE) برای هر روش ضروری است. (American Society of Echocardiography Springer)
🧱همبستگی متقاطع بلوکی Block Matching
روش Block Matching یک روش ساده و مؤثر برای برآورد جابجایی محلی در تصاویر متوالی است. تصویر به بلوکهای کوچک تقسیم میشود و برای هر بلوک در فریم مرجع، در فریم بعدی جستجو میشود که کدام بخش بیشترین شباهت را با آن بلوک دارد. جابجایی بین موقعیتهای متناظر بهعنوان بردار حرکت آن بلوک در نظر گرفته میشود و از مجموعه این بردارها میدان جابجایی ساخته میشود.
گامهای عملی الگوریتم
- تقسیم تصویر به بلوکها: تصویر به بلوکهای مربعی یا مستطیلی با اندازه مشخص تقسیم میشود. هر بلوک نماینده یک ناحیه محلی از بافت است که الگوی لکهای آن دنبال میشود.
- تعریف پنجره جستجو: برای هر بلوک در فریم مرجع، در فریم بعدی یک ناحیه جستجو تعیین میشود که انتظار میرود بلوک در آن جابهجا شده باشد.
- محاسبه معیار تطابق: برای هر موقعیت ممکن در پنجره جستجو، میزان شباهت بین بلوک مرجع و بلوک هدف محاسبه میشود. معیارهای رایج شامل اختلاف مربعات (حساس به تغییر روشنایی) و همبستگی نرمالشده (مقاومتر در برابر تغییرات روشنایی) هستند.
- انتخاب بهترین تطابق: موقعیتی که بیشترین شباهت یا کمترین اختلاف را نشان دهد بهعنوان تطابق انتخاب میشود و بردار جابجایی محاسبه میگردد.
- تصحیح زیرپیکسلی: برای افزایش دقت، اطراف بهترین تطابق برازش محلی انجام میشود یا از اینترپولاسیون استفاده میشود تا جابجایی با دقت کمتر از یک پیکسل برآورد شود.
- تبدیل به استرین: پس از برآورد میدان جابجایی، با بررسی تغییرات فضایی این میدان، مقادیر استرین محاسبه میشوند.
پارامترهای کلیدی و مقادیر پیشنهادی در اکوکاردیوگرافی
- اندازه بلوک: معمولاً بین ۸ تا ۳۲ پیکسل؛ بلوکهای کوچک حساسیت فضایی بالاتر ولی نویزپذیرتر، بلوکهای بزرگ پایداری بیشتر ولی حساسیت منطقهای کمتر فراهم میکنند.
- شعاع پنجره جستجو: باید بزرگتر از بیشینه جابجایی بین دو فریم باشد؛ در اکو معمولاً ±۵ تا ±۲۰ پیکسل بسته به فریمریت و ضربان قلب.
- معیار تطابق: همبستگی نرمالشده برای شرایطی که روشنایی یا گین تغییر میکند مناسبتر است.
- چندمقیاسی Pyramid: برای جابجاییهای بزرگ از رویکرد چندمقیاسی استفاده شود (ابتدا در تصویر کوچکشده جستجو، سپس تصحیح در مقیاس اصلی).
- زیرپیکسلیسازی: برازش پارابولیک یا اینترپولاسیون فرکانسی برای دقت بهتر توصیه میشود.
- آستانه اعتماد: مقدار حداقلی برای معیار تطابق تعیین شود تا تطابقهای ضعیف رد شوند.
مزایا و کاربردهای مناسب
- سادگی و شفافیت مفهومی که پیادهسازی و بهینهسازی آن را آسان میکند.
- مقاومت نسبی در برابر نویز با انتخاب بلوک و معیار مناسب.
- قابلیت اجرا در زمان واقعی با بهینهسازی و پیادهسازی چندمقیاسی.
- مناسب برای شرایطی که حرکت عمدتاً در صفحه تصویربرداری است و الگوهای لکهای بین فریمها پایدارند.
محدودیتها و منابع خطا
- حرکت خارج صفحه: اگر بافت از صفحه تصویربرداری خارج شود، تطابق صحیح وجود نخواهد داشت.
- دکورلاسیون الگوها: تغییر شکل یا تغییر زاویه بازتاب میتواند الگوی لکهای را تغییر دهد و تطابق را گمراه کند.
- تأثیر تغییرات روشنایی و آرتیفکتها: تغییر گین یا سایهگذاری میتواند معیار تطابق را مخدوش کند.
- حساسیت به پارامترها: انتخاب نامناسب اندازه بلوک یا پنجره جستجو میتواند خطاهای بزرگ ایجاد کند.
- میدان حرکت ناپیوسته: خروجی ممکن است نویزی یا ناپیوسته باشد؛ نیاز به فیلتر زمانی یا منظمسازی دارد.
روشهای بهبود و کنترل کیفیت
- استفاده از چندمقیاس برای پوشش جابجاییهای بزرگ و کاهش هزینه محاسباتی.
- اعمال فیلتر زمانی یا فیلتر کالمن برای افزایش پایداری بردارهای حرکت در طول فریمها.
- محاسبه نقشه اعتماد (confidence map) بر اساس مقدار معیار تطابق و حذف یا علامتگذاری سگمنتهای کماعتماد.
- همزمانی با ECG و انتخاب فریمهای مشابه در ریتمهای نامنظم برای میانگینگیری.
- اعتبارسنجی با داده مرجع مانند فانتومهای حرکتی یا MRI‑tagging برای تعیین دقت و خطای سیستم.
مقایسه خلاصه با روشهای دیگر
- در برابر Optical Flow: Block Matching محلیتر و سادهتر است؛ Optical Flow میدان سرعت پیوستهتری میدهد اما حساستر به نویز و نیازمند حل معادلات گرادیان است.
- در برابر Speckle Tracking پیشرفته: روشهای پیشرفتهتر از مدلهای زمانی و منظمسازی استفاده میکنند و معمولاً پایداری و دقت بالاتری نسبت به پیادهسازی ساده Block Matching دارند.
- در برابر Tissue Doppler: TDI سرعت را در جهت محور پرتو اندازه میگیرد و زاویهپذیر است؛ Block Matching میدان دوبعدی جابجایی را فراهم میکند و زاویهپذیری کمتری دارد.
Block Matching یک ابزار پایه و کاربردی برای برآورد حرکت محلی در تصاویر اکو است که با تنظیم پارامترها و افزودن مراحل تصحیح میتواند نتایج قابلاطمینانی تولید کند. برای کاربرد بالینی، ترکیب آن با فیلترهای زمانی، نقشههای اعتماد و رویکردهای چندمقیاسی و نیز اعتبارسنجی با داده مرجع ضروری است.
✨الگوریتمهای ردیابی لکه ها(ُSTE)
Speckle Tracking Echocardiography (STE) روشی غیرتهاجمی برای اندازهگیری حرکت و تغییر شکل میوکارد است که از الگوهای طبیعی «لکه» در تصاویر B‑mode (تصاویر دوبعدی سیاه و سفید اکو دوبعدی) استفاده میکند تا میدان جابجایی و سپس کرنش (strain) و نرخ کرنش را استخراج کند. این روش امکان ارزیابی کمّی عملکرد منطقهای و لایهای میوکارد را فراهم میسازد و در بسیاری از کاربردهای بالینی برای کشف اختلالات زیر بالینی بهکار میرود.
لکهها نتیجه تداخل امواج بازتابی از ساختارهای ریز بافتی هستند که در تصویر B‑mode بهصورت الگوهای روشن و تاریک ظاهر میشوند. این الگوها نسبتاً پایدارند و میتوان آنها را بهعنوان «نشانههای طبیعی» بافت برای ردیابی حرکت محلی در فریمهای متوالی بهکار برد. پایداری و تمایز این الگوها شرط لازم برای برآورد میدان جابجایی است؛ تغییرات زاویه تابش، عمق یا کیفیت اکتساب میتواند الگوها را دکورله کند و دقت ردیابی را کاهش دهد. biomecardio.com
💻مراحل پردازش
- پیشپردازش : بهبود سیگنال و کاهش نویز، نرمالسازی شدت و حذف فریمهای آرتیفکتدار انجام میشود تا الگوهای لکهای قابلردیابیتر شوند.
- تقسیمبندی و تعریف ROI : مرزبندی اندوکارد و اپیکارد و تقسیمبندی سگمنتال برای محاسبات منطقهای ضروری است. منظور از ROI منطقه هدف (Region of Interest) است.
- ردیابی لکهها : الگوریتمهای مختلف (همبستگی بلوکی، جریان نوری، یا روشهای مبتنی بر ویژگی و یادگیری عمیق) الگوهای لکهای را در فریمهای متوالی دنبال میکنند و میدان جابجایی دوبعدی یا سهبعدی را برآورد میکنند.
- تصحیح زیرپیکسلی و منظمسازی : برای افزایش دقت از اینترپولاسیون زیرپیکسلی و روشهای منظمسازی فضایی-زمانی استفاده میشود تا میدان حرکت هموار و فیزیکپذیر شود.
- محاسبه کرنش و نرخ کرنش : از تغییرات فضایی میدان جابجایی، کرنش محلی استخراج و با بررسی تغییرات زمانی، نرخ کرنش محاسبه میگردد. این زنجیره پردازشی در عمل با پارامترهای اکتساب (فریمریت، رزولوشن) و معیارهای کیفیت ردیابی ترکیب میشود تا خروجیهای قابلاعتماد تولید شوند. Number Analytics
🧩تفاوتهای 2D‑STE و 3D‑STE و پیامدهای عملی
2D‑STE : بر پایه نماهای دوبعدی استاندارد عمل میکند و کرنش طولی، عرضی و شعاعی را از نماهای مختلف ترکیب میسازد. مزیت اصلی آن سادگی اکتساب و پردازش است اما محدودیت مهم، حساسیت به حرکت خارج صفحه و نیاز به ترکیب چند نما برای محاسبات سهبعدی است.
3D‑STE : از دادههای حجمی سهبعدی استفاده میکند و میدان جابجایی سهبعدی را مستقیماً برآورد مینماید؛ این رویکرد حرکت خارج صفحه را حذف میکند و تحلیل هندسه و پیچش قلب را دقیقتر میسازد اما نیازمند پروبهای ماتریکس، فریمریت پایینتر یا تکنیکهای ultrafast و محاسبات سنگینتر است. neocardiolab.com
📌مزایا، محدودیتها و منابع خطا
مزایا : حساسیت بالا به اختلالات منطقهای و آشکارسازی علائم ؛ امکان استخراج پارامترهای لایهای و پیچشی؛ کاربرد در پایش کاردیوکسیکوتوکسیته و پیشبینی پاسخ به درمان. Taylor & Francis
محدودیتها و منابع خطا : وابستگی به کیفیت تصویر و پنجره آکوستیک؛ تأثیر بارگذاری (preload/afterload) بر مقادیر کرنش؛ اختلاف مقادیر بین سازندگان بهدلیل تفاوت در پیادهسازی الگوریتمها؛ حساسیت به حرکت خارج صفحه در 2D‑STE؛ دشواری در ریتمهای نامنظم. در مواردی که نیاز به بافتنگاری مستقیم (مثلاً تفکیک اسکار از التهاب) یا دید آناتومیک دقیق وجود دارد، MRI یا TEE ارجحاند.
🧭اعتبارسنجی، کنترل کیفیت و نکات بالینی
اعتبارسنجی : مقایسه با روشهای مرجع مانند MRI‑tagging یا فانتومهای حرکتی برای تعیین خطای سیستم و محاسبه معیارهای عددی (MAE, RMSE) ضروری است. biomecardio.com
کنترل کیفیت در بالین : ثبت فریمریت، نماها، نسخه نرمافزاری و شاخصهای کیفیت ردیابی در گزارش؛ استفاده از همان دستگاه/نرمافزار برای پیگیری روندی؛ اعمال آستانههای اعتماد و حذف سگمنتهای کمکیفیت از محاسبات جهانی.
تفسیر بالینی : نتایج کرنش باید در متن EF، داپلر، بیومارکرها و وضعیت همودینامیک تفسیر شوند؛ تغییرات کوچک باید بر اساس روند زمانی و نه یک اندازهگیری منفرد ارزیابی شوند.
🌬️جریان نوری Optical Flow
Optical Flow بهمعنای برآورد میدان سرعت ظاهری پیکسلها بین دو فریم متوالی تصویر است؛ هر بردار در این میدان نشاندهنده جابجاییِ ظاهریِ یک نقطه تصویر در بازه زمانی کوتاه است. این روش در بینایی ماشین برای استخراج اطلاعات حرکت و در پردازش ویدئو برای ردیابی و تحلیل دینامیک صحنه کاربرد گسترده دارد. jonathanmugan.com eureka.patsnap.com
فروض پایه و مسئله ریاضیاتی به زبان ساده :
- ثبات روشنایی: فرض میشود شدت روشنایی یک نقطه با حرکت آن بین دو فریم ثابت میماند (intensity or brightness constancy). (jonathanmugan.com)
- حرکت کوچک و پیوسته: برای مشتقگیری زمانی و فضایی معمولاً فرض میشود جابجایی بین فریمها کوچک است؛ در غیر این صورت از رویکردهای چندمقیاسی استفاده میشود. (eureka.patsnap.com)
- مسئله کمبود اطلاعات (Aperture Problem): معادله حرکت محلی یک معادله با دو مجهول است و برای حل یکتا نیاز به قیود اضافی (محلی یا سراسری) وجود دارد. (jonathanmugan.com)
⚙️روشهای کلاسیک و تفاوتهای کلیدی
| روش | نوع قید | ویژگی اصلی | مناسب برای |
|---|---|---|---|
| Lucas–Kanade | قید محلی (پنجره کوچک) | حل سیستم معادلات خطی در هر پنجره محلی؛ مناسب حرکتهای کوچک | ردیابی نقاط محلی و شرایط با بافت کافی. mia.uni-saarland.de |
| Horn–Schunck | قید سراسری (همگنسازی میدان) | مینیممسازی تابع هزینه شامل خطای روشنایی و اصطلاح هموارسازی میدان | تولید میدان سرعت پیوسته؛ مناسب صحنههای همگن. mia.uni-saarland.de |
| پیرامید چندمقیاسی | ترکیبی | ابتدا در مقیاس پایین جابجایی کلی را برآورد و سپس تصحیح در مقیاسهای بالاتر | حرکتهای بزرگ یا تغییرات مقیاس؛ کاربرد در ویدئوهای با فریمریت پایین. eureka.patsnap.com |
⚙️جزئیات عملی روشهای اصلی
Lucas–Kanade (محلی) : در هر پنجره کوچک، معادله خطی حرکت از فرض ثبات روشنایی خطیسازی میشود و با کمترین مربعات حل میگردد. نیازمند بافت محلی کافی (گرادیان فضایی غیرصفر) است؛ در لبهها یا نواحی یکنواخت دچار ابهام میشود. jonathanmugan.com
Horn–Schunck (سراسری) : میدان سرعت با افزودن یک جمله هموارساز به تابع هزینه بهصورت همزمان در کل تصویر برآورد میشود؛ این هموارسازی مشکل aperture را کاهش میدهد اما ممکن است جزئیات محلی را صاف کند. mia.uni-saarland.de
پیرامید چندمقیاسی و ترکیبی : برای حرکتهای بزرگ یا تغییرات مقیاس، ابتدا تصویر را کوچک کرده و حرکت کلی را برآورد میکنند، سپس در مقیاسهای بالاتر تصحیح انجام میشود؛ این رویکرد هم پایداری و هم دامنه جابجایی قابلپذیر را افزایش میدهد. eureka.patsnap.com
⚙️کاربرد در اکوکاردیوگرافی و نکات تخصصی
- کاربرد: Optical Flow میتواند میدان سرعت پیسکلبهپیکسل را در تصاویر B‑mode برآورد کند و بهعنوان جایگزین یا مکمل برای Block Matching و Speckle Tracking بهکار رود. eureka.patsnap.com
- مزایا در اکو: تولید میدان سرعت پیوسته و تفکیک حرکتهای کوچک محلی؛ مناسب برای تحلیل دینامیک دیواره و استخراج نرخ استرین. eureka.patsnap.com
- محدودیتها در اکو: حساسیت به نویز و تغییرات روشنایی، مشکل حرکت خارج صفحه (out‑of‑plane motion)، و نیاز به فریمریت کافی برای حفظ فرض حرکت کوچک. در عمل ترکیب با پیشپردازش قوی و رویکردهای چندمقیاسی ضروری است. jonathanmugan.com eureka.patsnap.com
⚙️پیادهسازی و پارامترهای کلیدی
- پیشپردازش: فیلتر حذف نویز، نرمالسازی شدت و تقویت لبهها برای افزایش پایداری معادلات جریان نوری.
- اندازه پنجره (برای Lucas–Kanade): پنجره کوچک حساسیت فضایی را افزایش میدهد اما نویزپذیر است؛ پنجره بزرگتر پایداری میآورد اما جزئیات را از بین میبرد.
- ضریب هموارسازی (برای Horn–Schunck): کنترلکننده trade‑off بین پیوستگی میدان و تطابق با دادهها؛ مقدار بهینه بسته به نویز و بافت تصویر تنظیم میشود.
- چندمقیاسی: تعداد سطوح پیرامید و فاکتور کاهش مقیاس باید بر اساس بیشینه جابجایی و فریمریت انتخاب شود.
- زیرپیکسلیسازی: اینترپولاسیون و برازش محلی برای افزایش دقت زیرپیکسلی معمولاً لازم است.
- کنترل کیفیت: محاسبه خطای بازسازی روشنایی، نقشه اعتماد و فیلتر زمانی یا فیلتر کالمن برای حذف جهشهای ناگهانی توصیه میشود. jonathanmugan.com mia.uni-saarland.de
🧩اعتبارسنجی و توصیههای عملی
- اعتبارسنجی: مقایسه با دادههای مرجع (فانتومهای حرکتی یا MRI‑tagging) برای تعیین خطا و محاسبه معیارهایی مانند MAE و RMSE ضروری است. eureka.patsnap.com
- ترکیب روشها: در عمل، ترکیب Optical Flow با Block Matching یا روشهای مبتنی بر speckle و اعمال منظمسازی زمانی و فضایی بهترین تعادل بین دقت و پایداری را فراهم میآورد. eureka.patsnap.com jonathanmugan.com
🧬الگوریتمهای مبتنی بر مدل رفتار مکانیکی میوکارد
مدلهای فیزیکی و پارامتریک، حرکت و تغییر شکل میوکارد را با استفاده از توصیفهای مکانیکی (مانند سختی، الاستیسیته، ویسکوزیته و تنش فعال) نمایش میدهند و سپس پارامترهای این مدلها با دادههای تصویربرداری برازش میشوند تا خواص مکانیکی بافت و پاسخ آن به بارگذاری پیشبینی شود. این رویکرد پیوندی میان فیزیک بافت و مشاهدات بالینی فراهم میآورد و امکان استخراج پارامترهای زیستیفیزیکی را میسر میسازد. (Springer arXiv.org) انواع مدلهای رایج و ویژگیهای کلیدی :
- الاستیک خطی و شبهخطی : مدلهایی ساده که رابطه تنش‑کرنش را با پارامترهای ثابت (مانند مدول یانگ) توصیف میکنند؛ مناسب برای تحلیلهای اولیه یا نواحی با تغییرات کوچک کرنش.
- هایپرالاستیک (غیرخطی) : برای بافتهایی که رفتار غیرخطی دارند (مانند میوکارد در دامنههای بزرگ کرنش) بهکار میرود؛ توابع انرژی ذخیرهشده برای توصیف پاسخ الاستیک استفاده میشوند.
- ویسکوالاستیک و مدلهای زمانوابسته : برای توصیف رفتار وابسته به نرخ بارگذاری و میرایی انرژی؛ پارامترهایی مانند مؤلفههای ویسکوزیته و زمانهای ریلکساسیون معرفی میشوند. arXiv.org
- مدلهای فعال‑پاسیو (Electro‑mechanical) : ترکیب مکانیک با فعالسازی عضلانی ناشی از تحریک الکتریکی؛ شامل منبع تنش فعال وابسته به فاز سیکل قلبی یا مدلهای سلولی‑بنیاد. Springer
🎯هدفهای کاربردی مدلسازی
- استخراج پارامترهای مکانیکی: تعیین سختی موضعی، مؤلفههای ویسکوزیته، یا پارامترهای غیرخطی که میتوانند نشانگر فیبروز، اسکار یا تغییرات ساختاری باشند. Springer
- شبیهسازی پاسخ به بارگذاری: پیشبینی تغییرات کرنش و توزیع تنش تحت شرایط مختلف همودینامیک (تغییر فشار یا حجم) یا پس از مداخلات درمانی. Wiley Online Library
- تفکیک مکانیکی بافت سالم و پاتولوژیک: پارامترهای برازششده میتوانند بهعنوان بیومارکرهای مکانیکی برای تشخیص زودرس بیماریها بهکار روند. Springer
🧮فرآیند برازش پارامتریک و مسائل عددی
- تعریف مسئله معکوس: پارامترهای مدل بهعنوان مجهولات تعریف میشوند و هدف یافتن مقادیری است که خروجی مدل (جابجایی، کرنش، یا سیگنالهای قابلمشاهده) را بهخوبی با دادههای تصویربرداری مطابقت دهد.
- تابع هزینه و معیار برازش: معمولاً اختلاف بین میدانهای جابجایی یا کرنش مشاهدهشده و شبیهسازیشده کمینه میشود؛ معیارها میتوانند شامل خطای میانگین مربعات، معیارهای مبتنی بر ویژگیهای زمانی یا ترکیبی از چند معیار باشند.
- روشهای بهینهسازی: از روشهای گرادیانمحور (برای مدلهای پیوسته و مشتقپذیر) و الگوریتمهای مبتنی بر جستجوی تصادفی یا تکاملی (برای فضای پارامتری پیچیده یا غیرخطی) استفاده میشود.
- قیدها و منظمسازی: برای جلوگیری از بیشبرازش و ناپایداری عددی، قیدهای فیزیکی (مثلاً مثبتبودن پارامترها)، منظمسازی فضایی‑زمانی و محدودیتهای بیوفیزیکی اعمال میشوند.
- شناسایی عدم قطعیت: تحلیل حساسیت و برآورد عدم قطعیت پارامترها (مثلاً با روشهای بیزی یا بوتاسترپ) برای تفسیر بالینی ضروری است.
⚙️دادههای مورد نیاز و استراتژیهای ترکیب داده
- منابع داده: میدانهای جابجایی یا کرنش استخراجشده از اکوکاردیوگرافی (2D/3D‑STE)، MRI‑tagging یا تصویربرداری حجمی. (arXiv.org arXiv.org)
- همزمانی و شرایط مرجع: تعیین نقطه مرجع زمانی (مثلاً ابتدای دیاستول) و ثبت همزمان ECG برای همترازی فازی ضروری است.
- ترکیب چندمنظوره: ادغام دادههای اکو با MRI یا اطلاعات همودینامیک (فشار، حجم) میتواند برازش را پایدارتر و پارامترها را فیزیولوژیکتر کند. (Wiley Online Library)
⚙️اعتبارسنجی، محدودیتها و ملاحظات بالینی
- اعتبارسنجی با داده مرجع: مقایسه پارامترهای استخراجشده با نتایج MRI‑tagging، آزمایشهای فانتوم یا اندازهگیریهای آزمایشگاهی برای تعیین خطا و قابلیت اعتماد ضروری است. (arXiv.org)
- محدودیتهای مدلسازی: میوکارد بافتی غیرخطی، ناهمسانگرد و ساختاری پیچیده است؛ مدلهای ساده ممکن است نتایج فیزیولوژیک ناقص تولید کنند و مدلهای پیچیده نیازمند داده و محاسبات سنگیناند. (Springer)
- وابستگی به کیفیت داده: خطا در میدان جابجایی یا کرنش ورودی (ناشی از نویز، حرکت خارج صفحه یا آرتیفکت) مستقیماً بر پارامترهای برازششده تأثیر میگذارد.
- تفسیر بالینی: پارامترهای مکانیکی باید در متن بالینی (فشار خون، داروها، وضعیت بارگذاری) تفسیر شوند؛ تغییرات پارامتری لزوماً نشاندهنده آسیب ساختاری نیست مگر در ترکیب با سایر شواهد.
⚙️پیادهسازی
- از مدلهای سلسلهمراتبی استفاده میشود: ابتدا مدلهای ساده برای برآورد اولیه و سپس افزایش پیچیدگی در صورت نیاز به تفسیر دقیقتر.
- پیشپردازش و کنترل کیفیت داده پیش از برازش انجام میشود؛ نقشههای اعتماد و حذف نواحی کمکیفیت ضروری است.
- تحلیل حساسیت و عدم قطعیت برای هر پارامتر گزارش میشود تا قابلیت اعتماد نتایج مشخص گردد.
- اعتبارسنجی چندمنظوره با MRI یا فانتومها و گزارش معیارهای عددی (MAE, RMSE) انجام شود. Springer arXiv.org
🔄الگوریتم های مبتنی بر پردازش دینامیک سیستم
فیلترهای حالتسنج (filtering) برای برآورد حالتهای پنهان دینامیکی سیستم از مشاهدات نویزی بهکار میروند. در زمینه ردیابی پویا در تصاویر پزشکی، حالتها معمولاً شامل موقعیت، جابجایی و سرعت محلی بافت هستند و مشاهدات از الگوریتمهای ردیابی لکه یا اندازهگیریهای تصویری حاصل میشود. هدف کاهش نویز، پر کردن شکافهای موقتی در ردیابی و تولید میدان حرکت پیوسته و سازگار با فیزیک مسئله است. Wikipedia MIT – Massachusetts Institute of Technology
🌟ایده پایه فیلتر کالمن
فیلتر کالمن یک برآوردگر بازگشتی است که با فرض مدل خطی دینامیکی و نویز گاوسی، بهترین برآورد میانگین مربعات خطا را برای حالت سیستم ارائه میدهد. این فیلتر دو گام اصلی دارد: پیشبینی (propagation) حالت بر اساس مدل دینامیکی و بهروزرسانی (correction) با استفاده از مشاهدات جدید. در شرایط فرضی، فیلتر کالمن مینیممکننده و بهینه است. Wikipedia CMU School of Computer Science
ساختار مدل
- معادله حالت دینامیکی: حالت در گام بعدی از حالت فعلی و ورودیهای کنترلی (در صورت وجود) تولید میشود.
- مدل مشاهده: مشاهدات تصویری تابعی خطی از حالت بهاضافه نویز اندازهگیری هستند.
- پارامترهای آماری: کوواریانس نویز فرآیند و نویز مشاهده که میزان اطمینان مدل و اندازهگیری را تعیین میکنند.
گامهای عملی
- پیشبینی: حالت و عدم قطعیت آن براساس مدل دینامیکی و کوواریانس نویز فرآیند پیشبینی میشود.
- محاسبه گین کالمن: نسبت عدم قطعیت پیشبینیشده به مجموع عدم قطعیت پیشبینی و عدم قطعیت مشاهده تعیین میشود.
- بهروزرسانی: با مشاهده جدید، حالت تصحیح و عدم قطعیت کاهش مییابد.
مزایا و محدودیتها
- مزایا: کارآمد محاسباتی، بازگشتی (نیاز به نگهداری تاریخچه کامل ندارد)، و در شرایط خطی‑گاوسی بهینه است.
- محدودیتها: عملکرد ضعیف در حضور غیرخطیبودن مدل یا توزیعهای غیرگاوسی؛ در این موارد از تعمیمهایی مانند EKF/UKF یا فیلتر ذرات استفاده میشود. CMU School of Computer Science
🌟فیلتر ذرات Particle Filter
فیلتر ذرات یک روش نمونهگیری مبتنی بر بیز است که توزیع پسین حالت را با مجموعهای از نمونههای وزندار (ذرات) تقریب میزند. هر ذره یک نمونه از حالت ممکن است و وزن آن نشاندهنده احتمال نسبی آن نمونه با توجه به مشاهدات است. این روش برای مدلهای غیرخطی و نویز غیرگاوسی مناسب است. MIT – Massachusetts Institute of Technology
گامهای عملی
- نمونهگیری اولیه: ذرات از توزیع اولیه حالت نمونهبرداری میشوند.
- پیشبینی ذرات: هر ذره بر اساس مدل دینامیکی و نمونهای از نویز فرآیند بهروزرسانی میشود.
- وزندهی: برای هر ذره، احتمال مشاهده فعلی دادهشده حالت ذره محاسبه و وزنگذاری میشود.
- نرمالسازی و بازنمونهگیری: وزنها نرمال میشوند؛ در صورت تمرکز وزنها روی تعداد کمی ذره، بازنمونهگیری انجام میشود تا تنوع ذرات حفظ شود.
مزایا و محدودیتها
- مزایا: قابلیت مدلسازی توزیعهای چندقلهای و غیرخطی، مقاومت در برابر مشاهدات غیرمعمول و گمشدن موقت ویژگیها.
- محدودیتها: هزینه محاسباتی بالا (نیاز به تعداد زیادی ذره برای تقریب دقیق)، حساسیت به طراحی تابع وزن و بازنمونهسازی، و دشواری در ابعاد بالا. MIT – Massachusetts Institute of Technology
مقایسه خلاصه فنی
| ویژگی | Kalman Filter | Particle Filter |
|---|---|---|
| خطی/غیرخطی | مناسب خطی؛ تعمیم با EKF/UKF | مناسب غیرخطی ذاتی |
| نویز | فرض گاوسی | هر توزیع (غیرگاوسی) |
| خروجی | برآورد میانگین و کوواریانس | تقریب توزیع کامل با ذرات |
| پیچیدگی محاسباتی | کم تا متوسط | متوسط تا زیاد (بسته به تعداد ذرات) |
| مقاومت به گمشدن ویژگی | محدود؛ نیاز به مدل قوی | بهتر؛ بازنمونهسازی میتواند بازیابی کند |
| کاربرد در اکو | ردیابی پیوسته با مدل دینامیکی ساده | ردیابی در شرایط پیچیده، occlusion یا توزیع چندقلهای |
🌟نکات عملی برای ردیابی پویا در اکوکاردیوگرافی
- تعریف حالت و مدل مشاهده: حالت میتواند شامل موقعیت، سرعت و شتاب محلی باشد؛ مدل مشاهده باید رابطه بین حالت و خروجیهای ردیابی (مثلاً جابجایی بلوک یا ویژگی تصویری) را مشخص کند.
- مقداردهی اولیه و نرمالسازی: مقداردهی اولیه دقیق و تعیین کوواریانسهای مناسب برای فیلتر کالمن یا توزیع اولیه و تعداد ذرات برای فیلتر ذرات حیاتی است.
- تنظیم پارامترها: کوواریانس نویز فرآیند و مشاهده (در کالمن) یا تابع وزن و استراتژی بازنمونهسازی (در ذرات) باید بر اساس نویز تصویر، فریمریت و انتظار حرکت تنظیم شوند.
- ادغام با نقشه اعتماد: خروجیهای معیار کیفیت ردیابی (مثلاً NCC یا confidence map) میتوانند بهعنوان مشاهدات یا برای وزندهی ذرات استفاده شوند تا گمشدن موقت ویژگیها بهتر مدیریت شود.
- منظمسازی زمانی و فضایی: فیلترهای زمانی (مثلاً کالمن) یا پسپردازش فضایی (هموارسازی میدان حرکت) برای حذف جهشهای ناگهانی و تولید میدان حرکت فیزیکپذیر توصیه میشود.
- پیادهسازی کارآمد: برای زمان واقعی، از پیادهسازی موازی، کاهش بعد حالت، یا ترکیب روشها (مثلاً کالمن برای بخش خطی و ذرات برای بخش غیرخطی) استفاده شود. publish.illinois.edu CMU School of Computer Science
🌟اعتبارسنجی و ارزیابی عملکرد
- معیارهای عددی: RMSE، MAE و توزیع خطا بین میدانهای جابجایی/استرین برآوردشده و مرجع (فانتوم یا MRI‑tagging) گزارش شود.
- آزمونهای سناریویی: سناریوهای با نویز افزوده، گمشدن موقت ویژگی و حرکت خارج صفحه باید برای سنجش پایداری و بازیابی الگوریتم اجرا شوند.
- تحلیل حساسیت: بررسی حساسیت پارامترها (کوواریانسها، تعداد ذرات، آستانهها) و برآورد عدم قطعیت پارامتری برای تفسیر بالینی ضروری است. MIT – Massachusetts Institute of Technology CMU School of Computer Science
🔁روشهای منظمسازی و حلمعکوس
این بخش روشهایی را توضیح میدهد که برای پایدارسازی و سادهسازی حل مسائل معکوس در برآورد میدان جابجایی بهکار میروند. هدف جلوگیری از نوسانات غیرواقعی، حذف نویز و کاهش پیچیدگی محاسباتی است تا جوابهای بهدستآمده هم پایدار و هم فیزیولوژیک باشند.
⚙️Tikhonov Regularization به زبان ساده
- چه کاری انجام میدهد: از رشد ناگهانی و نوسانات جواب جلوگیری میکند و جواب را «نرم» و پیوسته نگه میدارد.
- چطور عمل میکند: علاوه بر تلاش برای مطابقت با دادهها، یک مجازات برای جوابهای خیلی بزرگ یا خیلی ناپیوسته اعمال میشود تا راهحلهای معقولتر انتخاب شوند.
- چه زمانی مناسب است: وقتی انتظار میرود میدان جابجایی نسبتاً هموار باشد و جزئیات تیز چندانی وجود نداشته باشد.
- محدودیت عملی: ممکن است گذارهای واقعی و لبههای فیزیولوژیک را بیش از حد صاف کند؛ نیاز به تنظیم میزان مجازات دارد.
⚙️Total Variation به زبان ساده
- چه کاری انجام میدهد: نویزهای کوچک و نوسانات تصادفی را حذف میکند در حالی که گذارها و لبههای واقعی را حفظ مینماید.
- چطور عمل میکند: بهجای مجازات اندازه کلی جواب، مجازات روی تغییرات محلی جواب اعمال میشود تا بخشهای صاف حفظ و لبهها برجسته بمانند.
- چه زمانی مناسب است: وقتی میدان جابجایی انتظار میرود شامل نواحی با تغییرات ناگهانی یا مرزهای مشخص باشد (مثلاً مرز بین بافت سالم و اسکار).
- محدودیت عملی: حل عددی پیچیدهتر و محاسباتیتر است و گاهی جواب را بهصورت قطعهای نشان میدهد که نیاز به تنظیم و پسپردازش دارد.
⚙️SVD و PCA برای کاهش بعد و حذف نویز به زبان ساده
- چه کاری انجام میدهند: دادههای بزرگ را به مؤلفههای اصلی تقسیم میکنند و مؤلفههای کماهمیت (معمولاً نویز) را حذف میکنند.
- چطور عمل میکنند: الگوهای غالب در مجموعه داده شناسایی و نگه داشته میشوند؛ اجزای ضعیف و پراکنده که اغلب نویز هستند حذف میشوند.
- چه زمانی مناسب است: وقتی مجموعه داده بزرگ و نویزی است و نیاز به کاهش ابعاد قبل از حل معکوس یا برازش پارامتریک وجود دارد.
- محدودیت عملی: مؤلفههای نگهداشتهشده همیشه معادل ویژگیهای فیزیولوژیک نیستند؛ در دادههای بسیار غیرخطی ممکن است روشهای غیرخطی بهتر عمل کنند.
⚙️پردازش برآورد میدان جابجایی
- پیشپردازش: حذف نویز پایه و اصلاح شدت تصویر.
- کاهش بعد: اعمال SVD/PCA برای حذف مؤلفههای نویزی و کاهش ابعاد مسئله.
- حل معکوس با منظمسازی: انتخاب منظمسازی متناسب با ساختار مورد انتظار — هموار بودن → Tikhonov؛ حفظ لبهها → Total Variation.
- تنظیم پارامترها: تعیین میزان منظمسازی با روشهای عددی یا اعتبارسنجی تجربی تا تعادل بین تطابق با داده و هموارسازی برقرار شود.
- اعتبارسنجی و کنترل کیفیت: مقایسه با مرجع (فانتوم یا داده مرجع)، گزارش معیارهای خطا و تحلیل حساسیت پارامتری.
🤖روشهای دادهمحور و یادگیری ماشین
این بخش مجموعه روشهای مبتنی بر داده را برای تحلیل تصاویر اکو و استخراج پارامترهای عملکردی قلب (مانند استرین، میدان جابجایی و طبقهبندی بالینی) تشریح میکند. محور اصلی بر دو رویکرد است: ویژگیهای دستی و مدلهای سنتی که روی توصیفهای مهندسیشده تکیه دارند، و یادگیری عمیق که ویژگیها را مستقیماً از داده میآموزد. هر رویکرد مزایا، محدودیتها و نیازمندیهای دادهای خاص خود را دارد و انتخاب مناسب بستگی به هدف بالینی، حجم و کیفیت داده و نیاز به تفسیرپذیری دارد.
🎼ویژگیهای مدلهای یادگیری سنتی
مفهوم و جریان کاری:
- استخراج ویژگی: ابتدا از تصاویر یا سیگنالهای زمانی ویژگیهای معنیدار استخراج میشود؛ نمونهها شامل مقادیر استرین سگمنتال، شاخصهای زمانی (زمان اوج انقباض)، آماری محلی (میانگین، واریانس)، و ویژگیهای فرکانسی یا شکل موج است.
- مدلسازی سنتی: این ویژگیها به مدلهای کلاسیک مانند SVM، Random Forest و Gradient Boosting داده میشوند تا وظایفی مانند طبقهبندی بیماری، پیشبینی پاسخ درمان یا خوشهبندی بیماران انجام شود.
- چرایی کاربرد: این روشها زمانی مناسباند که داده برچسبخورده محدود است و نیاز به تفسیرپذیری نسبی وجود دارد.
مزایا و محدودیتها
- مزایا: شفافیت نسبی؛ نیاز کمتر به دادههای برچسبخورده؛ پیادهسازی و آموزش سریعتر؛ امکان استفاده از دانش بالینی در طراحی ویژگیها.
- محدودیتها: وابستگی به کیفیت و جامعیت ویژگیهای استخراجشده؛ دشواری در کشف الگوهای پیچیده و غیرخطی که در داده تصویری پنهاناند.
⚖️مقایسه سریع مدلهای سنتی
| روش | قابلیت تفسیر | نیاز به داده برچسبخورده | مقاومت به نویز | کاربرد معمول |
|---|---|---|---|---|
| SVM | بالا | کم تا متوسط | خوب برای دادههای با مرز مشخص | طبقهبندی دودویی با ویژگیهای مهندسیشده |
| Random Forest | متوسط | کم | مقاوم به نویز و اوتلایر | طبقهبندی چندکلاسه، اهمیت ویژگی |
| Gradient Boosting | پایینتر | متوسط | بسیار قوی در مدلسازی روابط غیرخطی | پیشبینی پیوسته و طبقهبندی با دقت بالا |
🧬شبکههای عصبی کانولوشنی CNN برای تحلیل تصویر
شبکههای کانولوشنی ویژگیها را خودکار میآموزند و قادرند الگوهای پیچیده فضایی و بافتی را از تصاویر استخراج کنند. این توانایی امکان برآورد مستقیم استرین، segmentation و حتی میدان جابجایی را فراهم میآورد بدون نیاز به طراحی دستی ویژگیها.
معماریهای متداول و نقش هر کدام
- U‑Net: مناسب نگاشت پیکسلی؛ برای segmentation و تخمین میدانهای پیکسلی (مثلاً نقشه استرین یا جریان) استفاده میشود. ساختار encoder‑decoder با اتصالات skip امکان حفظ جزئیات مکانی را میدهد.
- ResNet: مناسب استخراج ویژگیهای عمیق و نمایندگیهای سطح بالا؛ میتواند بهعنوان backbone برای وظایف طبقهبندی یا بهعنوان بخش استخراج ویژگی در شبکههای پیچیدهتر بهکار رود.
- معماریهای اختصاصی: شبکههای چندفریم یا شبکههایی که اطلاعات زمانی را هم میگیرند (مثلاً ConvLSTM) برای تحلیل دینامیک قلب مفیدند.
🌟مزایا و محدودیتها
- مزایا: توانایی یادگیری الگوهای پیچیده؛ عملکرد برتر در صورت وجود داده کافی؛ امکان انتها‑به‑انتها (تصویر → پارامتر).
- محدودیتها: نیاز به مجموعههای بزرگ برچسبخورده؛ خطر بیشبرازش؛ تفسیرپذیری کمتر نسبت به مدلهای سنتی؛ حساسیت به توزیع داده و تفاوت بین سازندگان دستگاه.
🔁یادگیری عمیق برای ردیابی حرکت و برآورد میدان جابجایی
شبکههای Optical Flow و ردیابی حرکت :
- شبکههای پیشبینی میدان حرکت: مدلهایی مانند FlowNet و PWC‑Net مستقیماً میدان سرعت یا جابجایی بین دو فریم را پیشبینی میکنند. این شبکهها با دادههای جفتشده (فریم۱، فریم۲ → میدان مرجع) آموزش مییابند و میتوانند جایگزین یا تکمیلکننده روشهای کلاسیک مانند Block Matching یا Optical Flow سنتی شوند.
- ویژگیها: سرعت پیشبینی بالا پس از آموزش؛ قابلیت یادگیری الگوهای پیچیده حرکت؛ نیاز به داده مرجع برای آموزش نظارتشده.
شبکههای ترکیبی فیزیک‑داده :
- ایده: قوانین مکانیکی (مثلاً محدودیتهای پیوستگی، محدودیتهای فیزیکی تنش‑کرنش) در تابع هزینه یا ساختار شبکه وارد میشوند تا خروجیها فیزیکپذیرتر شوند.
- مزایا: کاهش خطاهای غیرفیزیکی، نیاز کمتر به دادههای برچسبخورده کامل، افزایش تعمیمپذیری در شرایطی که داده واقعی محدود است.
- پیادهسازی: افزودن جریمههای فیزیکی به تابع هزینه، یا استفاده از ماژولهای شبیهساز فیزیکی در مسیر پیشبینی.
⚙️ملاحظات عملی
- حجم و کیفیت داده: اگر مجموعه برچسبخورده بزرگ در دسترس است، یادگیری عمیق معمولاً عملکرد بهتری میدهد؛ در غیر این صورت مدلهای سنتی یا روشهای ترکیبی مناسبترند.
- نیاز به تفسیرپذیری: برای تصمیمات بالینی که نیاز به توضیح دارند، مدلهای سنتی یا روشهای شفافتر ترجیح داده میشوند.
- افزایش داده و تعمیمپذیری: استفاده از افزونههای داده (augmentation)، انتقال یادگیری (transfer learning) و fine‑tuning برای کاهش نیاز به دادههای برچسبخورده.
- اعتبارسنجی و کنترل کیفیت: تقسیم داده به مجموعههای آموزشی/اعتباری/آزمون، اعتبارسنجی متقاطع، و ارزیابی با معیارهای بالینی (مثلاً RMSE برای میدان جابجایی، AUC برای طبقهبندی).
- پیادهسازی بالینی: نیاز به استانداردسازی نماها، ثبت همزمان ECG، و گزارش متادیتا برای قابلیت تکرار و پیگیری روندی بیمار.
- برای مطالعات اکتشافی یا با داده محدود: استخراج ویژگیهای دستی و استفاده از Random Forest یا Gradient Boosting پیشنهاد شدهاست.
- برای برآورد پیکسلی یا میدان حرکت: شبکههای U‑Net و Optical Flow CNNs مناسباند؛ در صورت امکان، ترکیب با محدودیتهای فیزیکی توصیه شدهاست.
- برای کاربردهای بالینی نیازمند تفسیر: مدلهای ترکیبی که خروجیهای شبکه را با ویژگیهای مهندسیشده تلفیق میکنند، تعادل مناسبی بین دقت و شفافیت فراهم میآورند.
- اعتبارسنجی: همیشه با فانتوم یا داده مرجع و آزمونهای بینناظری/درونناظری اعتبارسنجی انجام شود.
💻چالشهای یادگیری ماشین در اکو استرین
📝نیاز به داده برچسبخورده: چالش اصلی این است که مدلهای یادگیری عمیق برای یادگیری الگوهای پیچیده به مجموعههای بزرگ و باکیفیت از دادههای برچسبخورده نیاز دارند؛ برچسبها میتوانند شامل نقشههای استرین مرجع، میدانهای جابجایی یا برچسبهای تشخیصی بالینی باشند. کمبود دادههای برچسبخورده باعث میشود مدلها یا اصلاً یاد نگیرند یا بهسرعت بیشبرازش کنند. (arXiv.org MDPI) راهکارهای متداول شامل استفاده از فانتومها و دادههای شبیهسازیشده برای تولید ground truth، انتقال یادگیری از مجموعههای بزرگتر، و روشهای کمبرچسب (semi‑supervised) یا بدوننظارت است که تلاش میکنند نیاز به برچسب را کاهش دهند. (arXiv.org)
📝تعمیمپذیری بین دستگاهها و مراکز تصویربرداری : مسئله این است که تصاویر تولیدشده توسط پروبها و سازندگان مختلف، تنظیمات گین و فیلترهای متفاوت، و پروتکلهای اکتساب ناهمگن هستند؛ مدلی که روی دادههای یک مرکز آموزش دیده ممکن است روی دادههای مرکز دیگر عملکرد ضعیفی نشان دهد. این مشکل تعمیمپذیری یکی از موانع اصلی کاربرد بالینی مدلهاست. Springer Nature
📝اقدامات کاهش ریسک: شامل استانداردسازی پروتکلهای اکتساب، نرمالسازی پیشپردازش تصویر، استفاده از دادههای چندمرکزی در آموزش، و تکنیکهای تطبیق دامنه (domain adaptation) یا تنظیم دقیق (fine‑tuning) روی دادههای محلی است. ارزیابی خارجی (external validation) روی مجموعههای مستقل باید بخشی از روند گزارش نتایج باشد. Springer Nature
📝بیشبرازش Overfitting و کنترل آن: ماهیت مشکل بیشبرازش زمانی رخ میدهد که مدل الگوهای نویزی یا ویژگیهای خاص مجموعه آموزشی را یاد میگیرد و در دادههای جدید عملکرد ضعیف دارد. در تصویربرداری پزشکی، اندازه کوچک مجموعهها و عدم تنوع نمونهها این خطر را تشدید میکند. (Nature) روشهای مقابله شامل تقسیم مناسب داده به مجموعههای آموزش، اعتبارسنجی و آزمون، استفاده از cross‑validation، افزایش داده (augmentation)، منظمسازی (regularization)، کاهش بعد با روشهایی مانند PCA و استفاده از early stopping است. گزارش معیارهای عملکرد روی مجموعههای خارجی و انتشار منحنیهای یادگیری برای شفافیت توصیه میشود. RSNA Publications Online MDPI
📝نیاز به استانداردسازی دادهها و متادیتا : بدون استانداردسازی نماها، فریمریت، رزولوشن، واحدهای فیزیکی و متادیتای مرتبط (نسخه نرمافزاری، تنظیمات پروب، همزمانی ECG)، مقایسه نتایج بین مطالعات و پیگیری روند بیمار غیرقابل اعتماد میشود. استانداردسازی باعث افزایش قابلیت تکرار، تسهیل اعتبارسنجی بینمرکزی و کاهش خطاهای ناشی از تفاوتهای اکتساب میشود. (Nature) اجزای یک پروتکل استاندارد باید شامل قالبهای ذخیرهسازی، حداقل مشخصات اکتساب (نماها، فریمریت حداقلی، عمق)، فرمت متادیتا، روشهای پیشپردازش اجباری و معیارهای کیفیت تصویر (مثلاً نقشه اعتماد) باشد. ثبت و گزارش این متادیتا در مطالعات و در محصولات بالینی ضروری است. (Springer MDPI)
🎯جمعبندی و توصیههای عملی برای پروژههای ML در اکوکاردیوگرافی
- برنامهریزی دادهمحور: پیش از طراحی مدل، برنامه جمعآوری داده شامل تنوع مراکز، پروتکلهای اکتساب و برچسبگذاری تعریف شود. arXiv.org
- اعتبارسنجی قوی: ارزیابی داخلی با cross‑validation و اعتبارسنجی خارجی روی مجموعههای مستقل انجام شود و معیارهای شفاف گزارش گردد. RSNA Publications Online Springer
- استانداردسازی و متادیتا: قالب گزارش و حداقلهای اکتساب تعیین و در تمام مراحل رعایت شود. Nature
- ترکیب روشها: در صورت کمبود داده، از ترکیب روشهای کلاسیک (ویژگیهای مهندسیشده) با یادگیری عمیق یا از شبکههای physics‑informed استفاده شود تا نیاز به برچسب کاهش یابد و فیزیکپذیری حفظ شود. arXiv.org MDPI