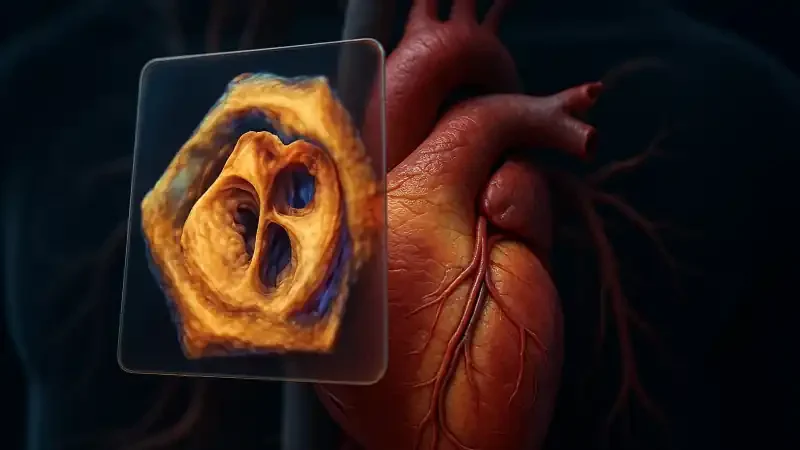
مقدمه
اکوکاردیوگرافی سهبعدی نسل جدید تصویربرداری قلب است که امکان مشاهده قلب را در شکل واقعی و حجمی فراهم میکند. این روش، دقت تشخیص بیماریهای دریچهای، ارزیابی عملکرد بطنها و بررسی نقصهای مادرزادی را بهطور چشمگیری افزایش میدهد. برخلاف اکو دوبعدی که تنها برشهایی محدود ارائه میدهد، اکو سهبعدی تصویر کاملی از قلب ارائه میکند و به پزشک اجازه میدهد ساختارها را از هر زاویه بررسی کند. این فناوری بهویژه در برنامهریزی و هدایت مداخلات قلبی مانند TAVI، MitraClip و بستن ASD نقش کلیدی دارد. استفاده از اکو سهبعدی در کلینیک ما به معنای ارائه دقیقترین و پیشرفتهترین ارزیابی قلبی برای بیماران است.
اکوکاردیوگرافی سهبعدی یکی از پیشرفتهترین روشهای تصویربرداری قلب با امواج فراصوت است که امکان مشاهده ساختارهای قلب را بهصورت حجمی و در زمان واقعی فراهم میکند. این فناوری بر پایه همان اصول فیزیکی اکوکاردیوگرافی کلاسیک بنا شده است، اما با استفاده از آرایههای چندبعدی حسگرها، دادههای بسیار گستردهتری را در یک برداشت جمعآوری میکند. نتیجه این فرایند، تصویری است که نهتنها سطح مقطع، بلکه حجم و شکل واقعی ساختارهای قلب را نشان میدهد. در این روش، امواج اولتراسوند از پروب دستگاه به سمت قلب ارسال میشوند و بازتاب آنها از بافتهای مختلف توسط حسگرهای متعدد دریافت میگردد. تفاوت مهم در این است که دستگاه سهبعدی میتواند حجم بزرگی از داده را در یک لحظه ثبت کند و سپس با استفاده از الگوریتمهای پردازش تصویر، یک مدل فضایی دقیق از قلب بسازد. این مدل امکان بررسی قلب از زوایای مختلف را فراهم میکند، بدون آنکه نیاز به تغییر موقعیت پروب باشد.
در مقایسه با اکوکاردیوگرافی دوبعدی، که تنها برشهایی تخت از قلب ارائه میدهد، نسخه سهبعدی اطلاعات بسیار کاملتری در اختیار پزشک قرار میدهد. در اکو دوبعدی، تفسیر تصویر تا حدی وابسته به تجربه پزشک و توانایی او در تصور ساختار سهبعدی قلب از روی تصاویر دوبعدی است. اما در اکو سهبعدی، این بازسازی ذهنی تا حد زیادی حذف میشود و خود دستگاه تصویر واقعیتری از آناتومی قلب ارائه میدهد. یکی از مهمترین مزایای این روش، ارزیابی دقیق عملکرد و ساختار دریچههای قلب است. دریچهها ساختارهایی پویا و پیچیده دارند و مشاهده آنها در قالب سهبعدی کمک میکند تا ناهنجاریهایی مانند نارسایی دریچهای، تنگی یا اختلال در حرکت لتها با دقت بیشتری تشخیص داده شود. این موضوع بهویژه در برنامهریزی درمانهای مداخلهای اهمیت دارد.
اکوکاردیوگرافی سهبعدی همچنین در اندازهگیری حجمهای قلب، مانند حجم پایانسیستول و پایاندیستول، دقت بالاتری دارد. در روشهای دوبعدی، این اندازهگیریها بر اساس فرضیات هندسی انجام میشود، اما در روش سهبعدی، حجم واقعی بطنها بدون نیاز به فرض شکل هندسی محاسبه میشود. این ویژگی برای ارزیابی عملکرد بطن چپ و راست بسیار ارزشمند است. این فناوری در بررسی نقصهای مادرزادی قلب نیز کاربرد گستردهای دارد. بسیاری از این ناهنجاریها شامل تغییرات پیچیده در ساختار دیوارهها، سپتومها و ارتباطات بین حفرهها هستند. مدل سهبعدی به پزشک اجازه میدهد مسیرهای جریان خون و شکل دقیق نقص را بهتر درک کند و تصمیمگیری درمانی دقیقتری داشته باشد.
یکی دیگر از کاربردهای مهم اکو سهبعدی، کمک به هدایت روشهای مداخلهای مانند ترمیم دریچه میترال، بستن نقصهای بینحفرهای یا قرار دادن دریچههای مصنوعی است. در این موارد، پزشک نیاز دارد موقعیت ابزارها و ساختارهای قلب را در لحظه ببیند و تصویر سهبعدی این امکان را فراهم میکند که مسیر حرکت ابزارها با دقت بیشتری کنترل شود. از نظر بالینی، انجام اکوکاردیوگرافی سهبعدی زمانی توصیه میشود که نیاز به ارزیابی دقیقتر ساختارهای قلب وجود داشته باشد یا زمانی که اکو دوبعدی نتواند اطلاعات کافی ارائه دهد. این روش بهویژه در بیمارانی که برای جراحی یا مداخله قلبی برنامهریزی میشوند، ارزش تشخیصی بالایی دارد.
برای کلینیک، ارائه این خدمت به معنای ارتقای سطح تشخیص و افزایش دقت در ارزیابی بیماران است. استفاده از این فناوری میتواند به کاهش خطاهای تشخیصی، بهبود برنامهریزی درمان و افزایش رضایت بیماران کمک کند. همچنین، امکان ذخیره و بازسازی تصاویر سهبعدی باعث میشود پزشکان بتوانند نتایج را با همکاران خود به اشتراک بگذارند و تصمیمگیری چندتخصصی بهتری داشته باشند.
🩺مزیتهای کلینیکی اکو سهبعدی
✅مشاهده قلب در شکل واقعی و بدون نیاز به حدس ذهنی : در اکو دوبعدی، پزشک باید از چند برش تخت، شکل سهبعدی قلب را در ذهن بازسازی کند. در اکو سهبعدی، خود دستگاه حجم واقعی قلب را نشان میدهد. این موضوع خطاهای ناشی از «تفسیر ذهنی» را بهطور چشمگیری کاهش میدهد.
✅ارزیابی بسیار دقیقتر دریچهها : اکو سهبعدی امکان مشاهده دریچهها را از زاویهای فراهم میکند که دقیقاً مشابه دید جراح در اتاق عمل است. این ویژگی باعث میشود محل دقیق پروولاپس یا پارگی لتها مشخص شود، شکل حلقه دریچه (annulus) بهطور کامل دیده شود، شدت و محل نارسایی دریچهای با دقت بیشتری تعیین گردد. این سطح از جزئیات در اکو دوبعدی قابلدستیابی نیست.
✅اندازهگیری حجم بطنها بدون فرض هندسی: در اکو دوبعدی، برای محاسبه حجم بطنها باید شکل آنها را «فرض» کرد (مثلاً بیضوی یا مخروطی). اما در اکو سهبعدی حجم بطن چپ و راست مستقیماً از حجم واقعی محاسبه میشود، کسر جهشی (EF) بسیار دقیقتر است، خطاهای ناشی از شکل غیرطبیعی بطنها حذف میشود و این موضوع در بیماران با کاردیومیوپاتی یا تغییر شکل بطن اهمیت حیاتی دارد.
✅تشخیص بهتر نقصهای مادرزادی قلب : اکو سهبعدی شکل و اندازه واقعی نقصهایی مانند ASD و VSD با مرزهای دقیق، ارتباط نقص با دریچهها و عروق، مسیرهای جریان خون در سه بعد را نشان میدهد. این اطلاعات برای برنامهریزی بستن نقصها ضروری است.
✅ارزیابی دقیقتر شدت نارسایی دریچهای: جتهای رگورژیتاسیون در واقع سهبعدی هستند، اما در اکو دوبعدی فقط یک «برش» از آنها دیده میشود. در اکو سهبعدی حجم واقعی جت، شکل و جهت آن، محل برخورد با دیوارهها همه بهصورت حجمی دیده میشود، بنابراین شدت نارسایی با دقت بیشتری تعیین میگردد.
✅کمک حیاتی در مداخلات ساختاری قلب : در روشهایی مانند MitraClip، TAVI ، بستن ASD/PFO ، قرار دادن دریچههای ترانسکاتتر، اکو سهبعدی نقش راهنما دارد و مسیر ابزارها و موقعیت دریچهها را در لحظه نشان میدهد. این موضوع ایمنی و موفقیت مداخله را افزایش میدهد.
✅کاهش نیاز به روشهای تهاجمیتر : به دلیل دقت بالا، در بسیاری از موارد نیاز به CT یا MRI کاهش مییابد، نیاز به کاتتریزاسیون تشخیصی کمتر میشود و این یعنی کاهش هزینه، زمان و ریسک برای بیمار.
✅گزارشدهی دقیقتر و قابلمقایسهتر: اکو سهبعدی امکان ذخیره حجم کامل قلب را فراهم میکند. پزشکان میتوانند حجم را دوباره بازسازی کنند، از زوایای جدید بررسی کنند، نتایج را با همکاران به اشتراک بگذارند و این موضوع کیفیت تصمیمگیری را بالا میبرد.
✅اکوکاردیوگرافی سهبعدی فقط یک «نسخه پیشرفتهتر» از اکو دوبعدی نیست، بلکه یک ابزار تشخیصی با تواناییهای کاملاً جدید است که:
- دقت تشخیص را افزایش میدهد
- برنامهریزی درمان را بهبود میبخشد
- مداخلات قلبی را ایمنتر میکند
- و در بسیاری از موارد، اطلاعاتی ارائه میدهد که هیچ روش دیگری قادر به ارائه آن نیست
🧭مقایسه اکو دوبعدی (۲D) و سهبعدی (۳D)
| موضوع مقایسه | اکوکاردیوگرافی دوبعدی (۲D) | اکوکاردیوگرافی سهبعدی (۳D) |
|---|---|---|
| نوع تصویر | برشهای تخت و محدود | تصویر حجمی و واقعی از قلب |
| نیاز به بازسازی ذهنی | زیاد – پزشک باید شکل قلب را حدس بزند | بسیار کم – شکل واقعی قلب دیده میشود |
| ارزیابی دریچهها | محدود، وابسته به زاویه | بسیار دقیق، امکان مشاهده از نمای «جراح» |
| اندازهگیری حجم بطنها | بر اساس فرض هندسی (بیضوی/مخروطی) | اندازهگیری مستقیم از حجم واقعی |
| دقت EF | متوسط، وابسته به کیفیت برشها | بسیار بالا، بدون فرض هندسی |
| بررسی نقصهای مادرزادی | گاهی ناکافی | نمایش کامل شکل و ارتباط نقصها |
| ارزیابی نارسایی دریچهای | مشاهده یک برش از جت | مشاهده حجم کامل جت و مسیر واقعی آن |
| کاربرد در مداخلات قلبی | محدود | ابزار راهنما در MitraClip، TAVI، ASD closure |
| ذخیره و بازسازی تصویر | فقط برشها ذخیره میشود | کل حجم ذخیره و قابل بازسازی است |
| کیفیت تصمیمگیری درمانی | خوب | بسیار عالی و دقیقتر |
🔎اصول علمی و فناوری مورد استفاده در اکوکاردیوگرافی سهبعدی
🪢مبانی فیزیکی امواج فراصوت
اکوکاردیوگرافی سهبعدی بر پایه همان اصول فیزیکی اکوکاردیوگرافی کلاسیک بنا شده است. در این روش، دستگاه امواج صوتی با فرکانس بالا (فراصوت) را به درون قفسه سینه ارسال میکند. این امواج پس از برخورد با بافتهای مختلف قلب، بازتاب مییابند و توسط حسگرهای موجود در پروب دریافت میشوند. تفاوت در چگونگی پردازش این بازتابهاست.
در اکو دوبعدی، بازتابها تنها برای ساخت یک «صفحه» از تصویر استفاده میشوند. اما در اکو سهبعدی، دستگاه حجم بزرگی از بازتابها را از زوایای مختلف جمعآوری میکند و با استفاده از الگوریتمهای پیچیده پردازش تصویر، یک مدل حجمی و واقعی از قلب میسازد. این مدل امکان مشاهده قلب از هر زاویه و در هر لحظه را فراهم میکند.
♨️پروب ماتریکس و نحوه عملکرد آن
پیشرفت اصلی اکو سهبعدی در نوع پروب آن نهفته است. برخلاف پروبهای معمولی که تنها یک ردیف حسگر دارند، پروب سهبعدی از آرایه ماتریکسی تشکیل شده است؛ یعنی صدها تا هزاران حسگر کوچک که در دو جهت افقی و عمودی چیده شدهاند.این آرایش باعث میشود پروب بتواند:
- امواج فراصوت را همزمان در چندین جهت ارسال کند
- بازتابها را از یک «حجم» کامل دریافت کند
- اطلاعات را در یک برداشت واحد جمعآوری کند
بهعبارت دیگر، پروب ماتریکس مانند یک دوربین چندچشمی عمل میکند که از هر نقطه قلب، اطلاعاتی سهبعدی بهدست میآورد. این فناوری امکان تصویربرداری حجمی در زمان واقعی را فراهم کرده و اساس اکو سهبعدی مدرن است.
🆚تفاوت برداشت حجمی با برداشت دوبعدی
در اکو دوبعدی، تصویر تنها یک «برش» از قلب است؛ مانند نگاهکردن به یک ساختمان از یک پنجره باریک. پزشک باید با کنار هم گذاشتن چند برش، شکل سهبعدی قلب را در ذهن بازسازی کند.اما در اکو سهبعدی:
- دستگاه یک حجم کامل از قلب را ثبت میکند
- تصویر قابل چرخش، برشزدن و مشاهده از هر زاویه است
- نیازی به حدسزدن شکل واقعی ساختارها نیست
این تفاوت باعث میشود:
- خطاهای ناشی از انتخاب اشتباه زاویه کاهش یابد
- ساختارهای پیچیده مانند دریچهها با دقت بسیار بیشتری دیده شوند
- اندازهگیریها دقیقتر و مستقل از فرضیات هندسی باشند
بهطور خلاصه، اکو دوبعدی «برش» میدهد، اما اکو سهبعدی «واقعیت» را نشان میدهد.
🫀انواع مدهای تصویربرداری سهبعدی
استانداردهای ASE و ESC چهار مد اصلی تصویربرداری سهبعدی را معرفی کردهاند. هر مد برای هدف خاصی طراحی شده است:
- تصویربرداری زنده (Real-time / Live 3D) با حجم کوچکتر، سرعت نمایش بالا، مناسب برای مشاهده لحظهای حرکات دریچهها و دیوارهها. این مد برای بررسی دینامیک قلب در زمان واقعی بسیار مفید است.
- حجم کامل (Full-volume 3D) که ترکیب چند ضربان قلب، حجم بزرگتر و رزولوشن بالاتر و بهترین روش برای اندازهگیری حجم بطنها و EF است. این مد حساس به آریتمی است، زیرا برای ترکیب ضربانها نیاز به ریتم منظم دارد.
- بزرگنمایی سهبعدی (3D Zoom) که تمرکز بر یک ساختار خاص، وضوح بالا در ناحیه محدود، استاندارد طلایی برای بررسی دریچه میترال و آئورت میباشد. این مد امکان مشاهده دریچهها از نمای «روبروی جراح» را فراهم میکند.
- داپلر رنگی سهبعدی (3D Color Doppler) که نمایش حجمی جریان خون، مشاهده شکل واقعی جتهای نارسایی، ارزیابی دقیقتر شدت رگورژیتاسیون را ممکن میسازد و در تشخیص نارساییهای دریچهای بسیار ارزشمند است.
ℹ️جمعآوری دادههای حجمی
در اکو دوبعدی، دستگاه فقط یک «صفحه» از قلب را در هر لحظه ثبت میکند؛ اما در اکو سهبعدی، هدف این است که یک حجم کامل از قلب یا بخشی از آن در یک بازه زمانی مشخص (معمولاً یک یا چند ضربان قلب) ثبت شود. این یعنی بهجای یک خط اسکن، با یک «میدان سهبعدی اسکن» سروکار داریم. در این مرحله، خروجی هنوز «تصویر» نیست؛ بلکه مجموعهای از دادههای خام است که بعداً به تصویر سهبعدی تبدیل میشود.
♨️نقش پروب ماتریکس در جمعآوری دادههای حجمی
کلید این مرحله، پروب ماتریکس (Matrix Array Transducer) است که بهجای یک ردیف المان (حسگر)، دارای آرایهای دوبعدی از صدها تا هزاران المان است. هر المان میتواند امواج فراصوت را ارسال و بازتابها را دریافت کند. دستگاه با فعالکردن گروههای مختلف از این المانها، پرتو را در جهات مختلف هدایت میکند. نتیجه این است که بهجای اسکن یک خط یا یک صفحه، یک «حجم» از فضا اسکن میشود. هر نقطه در آن حجم، یک پاسخ (اکو) دارد که در حافظه دستگاه ذخیره میشود. این مجموعه پاسخها همان دادههای حجمی (Volumetric Data) است.
🪟هندسه میدان دید و حجم برداشتشده
در عمل، دستگاه یک «هرم سهبعدی» یا «بخش مخروطیشکل» از قلب را اسکن میکند:
- رأس هرم: محل پروب روی قفسه سینه
- قاعده هرم: ناحیهای از قلب (مثلاً دریچه میترال یا کل بطن چپ)
- زاویه بازشدگی هرم: تعیینکننده پهنای میدان دید
هرچه زاویه بازشدگی و عمق بیشتر باشد:
- حجم بیشتری از قلب پوشش داده میشود
- اما رزولوشن زاویهای و فریمریت ممکن است کاهش یابد
بنابراین، در مرحله جمعآوری داده، همیشه یک توازن بین حجم پوششدادهشده و کیفیت/سرعت تصویر وجود دارد.


✅مدهای مختلف جمعآوری دادههای حجمی
در همین مرحله، نوع مد تصویربرداری تعیین میشود و این انتخاب، شکل دادههای حجمی را عوض میکند:
۱. مد زنده سهبعدی (Real-time / Live 3D)
- حجم کوچکتر
- فریمریت بالا
- مناسب برای مشاهده لحظهای حرکت دریچهها و دیوارهها
- دادههای حجمی در هر ضربان بهصورت پیوسته بهروزرسانی میشود
۲. مد حجم کامل (Full-volume 3D)
- چندین ضربان قلب پشتسرهم ثبت میشود
- هر ضربان، بخشی از حجم نهایی را تأمین میکند
- دستگاه این بخشها را با هم ترکیب میکند و یک حجم بزرگ و با رزولوشن بالا میسازد
- حساس به آریتمی: اگر ضربانها نامنظم باشند، حجم نهایی دچار اعوجاج میشود
۳. مد بزرگنمایی سهبعدی (3D Zoom)
- تمرکز روی یک ناحیه محدود (مثلاً فقط دریچه میترال)
- حجم کوچکتر، اما رزولوشن فضایی بالاتر
- برای بررسی دقیق آناتومی یک ساختار خاص استفاده میشود
۴. مد داپلر رنگی سهبعدی (3D Color)
- علاوه بر بازتاب بافت، اطلاعات سرعت جریان خون نیز در حجم ثبت میشود
- هر نقطه از حجم، هم «شدت بازتاب» دارد و هم «سرعت جریان»
- دادههای حجمی پیچیدهتر و سنگینتر میشوند، اما اطلاعات بسیار غنیتری فراهم میکنند
✅نقش ECG و تنفس در جمعآوری دادههای حجمی
برای اینکه دادههای حجمی قابلاعتماد باشند، دستگاه باید بداند:
- کدام لحظه از چرخه قلبی را ثبت میکند
- آیا ضربانها منظم هستند یا نه
به همین دلیل:
- سیگنال ECG همزمان ثبت میشود.
- در مد Full-volume، هر زیرحجم به یک فاز مشخص از چرخه قلبی نسبت داده میشود.
- اگر آریتمی وجود داشته باشد، ترکیب زیرحجمها ممکن است منجر به تصویر «تکهتکه» یا اعوجاجشده شود.
تنفس نیز مهم است:
- حرکت قفسه سینه میتواند موقعیت قلب را بین ضربانها تغییر دهد.
- در برداشتهای چندضربانی، معمولاً از بیمار خواسته میشود نفس خود را برای چند ثانیه حبس کند.
✅پارامترهای کلیدی در تنظیم جمعآوری دادههای حجمی
در این مرحله، اپراتور (تکنسین یا پزشک) باید چند پارامتر مهم را تنظیم کند:
- عمق (Depth): هرچه عمق بیشتر، حجم بزرگتر اما رزولوشن کمتر.
- پهنای میدان (Sector Width): هرچه پهنتر، پوشش بیشتر اما فریمریت پایینتر.
- Gain و Dynamic Range: برای جلوگیری از اشباع یا کمنور شدن ساختارها.
- Focus: تعیین ناحیهای که بیشترین وضوح را خواهد داشت.
این تنظیمات مستقیماً روی کیفیت دادههای حجمی اثر میگذارند و در استانداردهای ASE/ESC بهعنوان «پیششرطهای کیفیت» ذکر شدهاند.
✅خروجی این مرحله: دیتاست حجمی (3D Data Set)
در پایان مرحله جمعآوری دادههای حجمی، دستگاه یک دیتاست سهبعدی در اختیار دارد:
- این دیتاست شامل هزاران نقطه (Voxel) است که هرکدام شدت بازتاب (و در صورت داپلر، اطلاعات جریان) دارند.
- هنوز پردازشهای سنگین مثل بازسازی، رندرینگ، MPR و سگمنتیشن انجام نشده است.
- این دیتاست میتواند ذخیره شود و بعداً روی کنسول یا نرمافزارهای پیشرفته بازسازی و تحلیل گردد.
بهعبارت دیگر، این مرحله مثل گرفتن نگاتیو خام در عکاسی است؛ اگر نگاتیو خوب نباشد، هیچ ادیتی تصویر را نجات نمیدهد.
جمعآوری دادههای حجمی در اکوکاردیوگرافی سهبعدی یعنی:
- استفاده از پروب ماتریکس برای اسکن یک حجم کامل از قلب
- انتخاب مد مناسب (زنده، حجم کامل، بزرگنمایی، داپلر سهبعدی)
- هماهنگی با ECG و تنفس برای جلوگیری از اعوجاج
- تنظیم دقیق عمق، پهنای میدان و سایر پارامترها برای رسیدن به بهترین کیفیت
این مرحله، پایه و زیرساخت تمام آن چیزی است که بعداً بهصورت تصویر سهبعدی زیبا، قابلچرخش و قابلاندازهگیری دیده میشود.
✅تحلیل اطلاعات و تشکیل پرتو سه بعدی
مرحلهٔ «تشکیل پرتو سهبعدی» در اکوکاردیوگرافی، قلب تپندهٔ تمام فرایند تصویربرداری است؛ جایی که دستگاه میکوشد از دل انبوهی از بازتابهای صوتی، تصویری منسجم، دقیق و قابلاعتماد از ساختارهای قلبی بسازد. اگر مرحلهٔ نخست را گردآوری خام دادهها بدانیم، این مرحله همان جایی است که آن دادههای پراکنده، نظم مییابند و به تصویری سهبعدی بدل میشوند. در اکو دوبعدی، تشکیل پرتو تنها در یک صفحه انجام میشود؛ دستگاه پرتو را در یک جهت مشخص هدایت میکند و بازتابها را برای ساختن یک «برش» از قلب ترکیب مینماید. اما در اکو سهبعدی، این فرایند از یک صفحهٔ ساده به یک میدان سهبعدی گسترده ارتقا مییابد و همین تغییر، پیچیدگی محاسبات را چندین برابر میکند.
در اکو سهبعدی، دستگاه باید پرتوهای فراصوت را نهفقط در یک محور، بلکه در سه محور اصلی هدایت کند. این یعنی هر بار که دستگاه میخواهد نقطهای از قلب را ببیند، باید زاویهٔ افقی، زاویهٔ عمودی و عمق آن نقطه را بهطور همزمان محاسبه کند. پروب ماتریکس که دارای آرایهای دوبعدی از صدها یا هزاران المان است، این امکان را فراهم میسازد که پرتوها در هر جهت دلخواه شکل بگیرند. هر المان با تأخیر زمانی بسیار دقیق فعال میشود تا امواج در نقطهٔ موردنظر روی هم جمع شوند و تمرکز یابند. این تمرکز، که در اکو دوبعدی تنها در یک یا چند عمق محدود انجام میشد، در اکو سهبعدی باید برای لایههای متعدد و در زوایای گوناگون تکرار شود. بدین ترتیب، دستگاه برای هر نقطه از حجم، مجموعهای از محاسبات پیچیدهٔ زمانبندی و ترکیب سیگنال را انجام میدهد.
در این مرحله، دستگاه با سیلی از بازتابها روبهروست. هر المان پروب بازتاب امواج را با شدت و زمان متفاوت دریافت میکند و دستگاه باید تشخیص دهد که هر بازتاب متعلق به کدام نقطه از حجم است. این کار در اکو دوبعدی نسبتاً ساده است، زیرا تنها یک صفحهٔ باریک اسکن میشود؛ اما در اکو سهبعدی، دستگاه باید بازتابها را از هزاران مسیر ممکن تحلیل و طبقهبندی کند. هر نقطه از حجم سهبعدی نتیجهٔ ترکیب هوشمندانهٔ بازتابهایی است که از دهها یا صدها المان دریافت شدهاند. این حجم عظیم از محاسبات، بار پردازشی سنگینی ایجاد میکند و همین امر سبب شده است که تشکیل پرتو سهبعدی یکی از دشوارترین و پرهزینهترین مراحل پردازش در اکو باشد.
در نسلهای نخستین اکو سهبعدی، توان پردازشی دستگاهها محدود بود. پردازندههای آن زمان قادر نبودند این حجم از محاسبات را در زمان واقعی انجام دهند؛ بنابراین تصاویر سهبعدی کند، کوچک و گاه پر از نویز بودند. دستگاهها ناچار بودند حجم تصویربرداری را کوچک کنند یا از برداشتهای چندضربانی استفاده کنند تا بتوانند دادهها را با سرعت قابلقبول پردازش نمایند. اما با پیشرفت فناوری، پردازندههای موازی، واحدهای پردازش سیگنال اختصاصی و حتی پردازندههای گرافیکی داخلی وارد میدان شدند. این تحول موجب شد که دستگاهها بتوانند دهها یا صدها خط سهبعدی را بهطور همزمان پردازش کنند و تصویری روان، زنده و باکیفیت ارائه دهند.
بهبیان دیگر، آنچه امروز بهعنوان «اکوی سهبعدی زنده» میشناسیم، نتیجهٔ سالها پیشرفت در معماری پردازندهها و الگوریتمهای تشکیل پرتو است. اکنون دستگاهها قادرند حجمهای بزرگتری را با وضوح بالاتر و در زمان واقعی بازسازی کنند؛ امری که در گذشته تنها یک آرزو بود. این مرحله، همچنان پیچیدهترین بخش فرایند تصویربرداری سهبعدی است و هر پیشرفتی در آن، مستقیماً کیفیت و دقت تصویر نهایی را ارتقا میدهد.
در اکوکاردیوگرافی سهبعدی، «تشکیل پرتو» همان جایی است که دستگاه تصمیم میگیرد کجا را ببیند، با چه دقتی ببیند و در چه عمقی تمرکز کند. اگر مرحله اول را جمعآوری خام دادهها بدانیم، مرحله دوم همان مغز ماجراست که از این دادهها یک میدان سهبعدی قابلاستفاده میسازد.

☑️Beamforming در ۲D چیست و چرا در ۳D پیچیدهتر میشود؟
در اکو دوبعدی، پروب یک ردیف المان دارد. دستگاه:
- پالس را از چند المان بهصورت هماهنگ میفرستد
- با تأخیرهای زمانی بسیار دقیق، جهت پرتو را در یک صفحه خاص تنظیم میکند
- بازتابها را از همان جهت دریافت و با هم ترکیب میکند تا یک «خط» از تصویر ساخته شود
- با تکرار این کار در زوایای مختلف، یک «صفحه» دوبعدی تشکیل میشود
پس در ۲D، Beamforming یعنی:
- هدایت پرتو در یک صفحه
- تمرکز در یک عمق مشخص
- ترکیب بازتابها برای ساختن یک خط تصویری
اما در ۳D، داستان از «یک صفحه» به «یک حجم» ارتقا پیدا میکند.
☑️ در ۳D، پرتو باید در سه محور هدایت شود
در پروب ماتریکس، المانها در دو جهت (X و Y) چیده شدهاند. این یعنی:
- دستگاه میتواند پرتو را نهفقط در یک صفحه، بلکه در هر جهت داخل یک هرم سهبعدی هدایت کند.
- بهجای اسکن یک خط، باید یک شبکه سهبعدی از خطوط را اسکن کند.
برای هر «خط سهبعدی» (Ray):
- باید تعیین شود در چه زاویه افقی (Azimuth) و چه زاویه عمودی (Elevation) پرتو حرکت کند.
- این یعنی Beamforming دیگر دوبعدی نیست، بلکه سهبعدی است.
به زبان ساده:
در ۲D، مثل این است که با چراغقوه فقط روی یک دیوار نور میاندازی.
در ۳D، باید کل اتاق را با همان چراغقوه، نقطهبهنقطه اسکن کنی.
☑️تمرکز (Focusing) در عمقهای مختلف
در ۲D:
- معمولاً یک یا چند «فوکوس» در عمقهای مشخص تنظیم میشود.
- پرتو در آن عمقها بیشترین وضوح را دارد.
در ۳D:
- چون حجم بزرگتری اسکن میشود، باید در چندین عمق و در چندین جهت فوکوس انجام شود.
- دستگاه باید برای هر جهت و هر عمق، تأخیرهای زمانی المانها را طوری تنظیم کند که امواج در آن نقطه خاص روی هم جمع شوند (Constructive interference).
این یعنی:
- تعداد محاسبات فوکوس در ۳D چندین برابر ۲D است.
- هر نقطه از حجم، نتیجه یک سری محاسبات دقیق زمانبندی و ترکیب سیگنال است.
☑️ ترکیب بازتابها از هزاران مسیر
هر المان پروب:
- بازتاب امواج را با زمان و شدت متفاوت دریافت میکند.
- دستگاه باید بداند کدام بازتاب مربوط به کدام نقطه از حجم است.
در ۲D:
- برای هر خط تصویری، تعداد محدودی المان درگیر هستند.
- ترکیب سیگنالها در یک بعد زاویهای انجام میشود.
در ۳D:
- برای هر «خط سهبعدی»، تعداد بیشتری المان درگیر میشوند.
- ترکیب سیگنالها در دو بعد زاویهای (Azimuth و Elevation) + عمق انجام میشود.
- تعداد مسیرهای ممکن برای رسیدن موج به پروب بسیار بیشتر است.
نتیجه:
Beamforming سهبعدی یعنی:
- محاسبه تأخیر زمانی برای صدها یا هزاران المان
- ترکیب هوشمند سیگنالها برای هر نقطه از حجم
- تکرار این کار برای هزاران نقطه در هر فریم
این همان چیزی است که این مرحله را سنگینترین بخش پردازش میکند.

☑️چرا این مرحله به پردازندههای بسیار سریع نیاز دارد؟
برای هر فریم سهبعدی:
- هزاران خط سهبعدی باید پردازش شوند.
- برای هر خط، صدها المان باید با تأخیرهای دقیق تنظیم و ترکیب شوند.
- این کار باید در زمان بسیار کوتاه انجام شود تا تصویر «زنده» بهنظر برسد.
اگر پردازنده کند باشد:
- فریمریت پایین میآید.
- تصویر سهبعدی «لَگ» پیدا میکند.
- استفاده بالینی از آن محدود میشود.
به همین دلیل، نسلهای اولیه اکو ۳D:
- فریمریت پایین
- حجم کوچک
- کیفیت محدود
داشتند، چون توان پردازشی کافی وجود نداشت.
☑️مسیر پیشرفت: از کند و محدود تا زنده و حجیم
نسلهای قدیمی:
- پردازندههای عمومی (CPU) با توان محدود
- Beamforming سهبعدی با سرعت پایین
- نیاز به برداشتهای طولانی و چندضربانی
- تأخیر زیاد بین برداشت و نمایش تصویر
نسلهای جدید:
- استفاده از پردازندههای موازی (Parallel Processing)
- استفاده از پردازندههای اختصاصی سیگنال (DSP) و GPU داخلی
- انجام همزمان محاسبات Beamforming برای چندین خط
- امکان Real-time 3D با حجمهای بزرگتر و فریمریت قابلقبول
به زبان ساده:
قبلاً دستگاه باید هر خط را جداگانه حساب میکرد؛
الان میتواند دهها یا صدها خط را همزمان پردازش کند.
☑️جمعبندی مرحله Beamforming سهبعدی
در مرحله تشکیل پرتو سهبعدی:
- دستگاه تصمیم میگیرد کدام نقطه از قلب را، در کدام جهت و در کدام عمق ببیند.
- برای این کار، باید زمانبندی ارسال و دریافت امواج در صدها یا هزاران المان را با دقت میکروثانیهای تنظیم کند.
- سپس بازتابها را طوری با هم ترکیب کند که هر نقطه از حجم، یک مقدار شدت مشخص داشته باشد.
این مرحله:
- قلب محاسباتی اکو سهبعدی است
- بیشترین بار پردازشی را دارد
- و پیشرفت آن، مستقیماً به پیشرفت سختافزار و معماری پردازندهها گره خورده است.
✅بازسازی حجمی اطلاعات
بازسازی حجمی در اکوکاردیوگرافی سهبعدی مرحلهای است که در آن دستگاه میکوشد از دل دادههای خام و پراکندهای که در مرحلهٔ تشکیل پرتو بهدست آمده، تصویری منسجم، پیوسته و قابلفهم از قلب بسازد. اگر مرحلهٔ Beamforming را بتوان «شنیدن» قلب دانست، بازسازی حجمی همان «دیدن» قلب است؛ یعنی تبدیل سیگنالهای صوتی به یک ساختار فضایی که بتوان آن را چرخاند، برش زد و از هر زاویه بررسی کرد. این مرحله، پلی است میان فیزیک امواج و ادراک بصری انسان.
در آغاز این فرایند، دستگاه با مجموعهای از نقاط سهبعدی روبهروست که هرکدام تنها یک مقدار شدت بازتاب دارند. این نقاط، مانند دانههای پراکندهٔ نور در فضایی تاریکاند؛ هنوز شکل و مرز مشخصی ندارند. نخستین وظیفهٔ دستگاه این است که این نقاط را در یک شبکهٔ منظم فضایی قرار دهد؛ شبکهای که در آن هر نقطه (یا «وُکسل») جایگاهی دقیق در سه بعد دارد. این مرحله نیازمند محاسبات هندسی پیچیده است، زیرا دستگاه باید بداند هر بازتاب دقیقاً از کدام نقطهٔ قلب آمده است و آن نقطه در چه فاصله و چه زاویهای نسبت به پروب قرار داشته است.
پس از این مرحلهٔ هندسی، دستگاه باید خلأهای میان دادهها را پر کند. هیچ دستگاهی نمیتواند تمام نقاط یک حجم را بهطور کامل اسکن کند؛ بنابراین میان نقاط واقعی، فضاهای خالی وجود دارد. الگوریتمهای بازسازی حجمی با استفاده از روشهایی مانند درونیابی سهبعدی، این فضاهای خالی را پر میکنند و تصویری پیوسته میسازند. این کار شبیه آن است که نقاشی بخواهد از میان چند نقطهٔ پراکنده، خطوط و سطوحی پیوسته ترسیم کند. هرچه الگوریتمها پیشرفتهتر باشند، تصویر نهایی طبیعیتر و دقیقتر خواهد بود.
در مرحلهٔ بعد، دستگاه باید مرزهای ساختارهای قلبی را از دل این حجم استخراج کند. قلب مجموعهای از سطوح پیچیده و منحنی است: دیوارههای بطنها، لتهای دریچهها، حلقهٔ میترال، سپتوم و… . الگوریتمهای بازسازی حجمی با تحلیل تغییرات شدت بازتابها، این مرزها را تشخیص میدهند و سطوحی سهبعدی میسازند که بتوان آنها را بهصورت رندر شده مشاهده کرد. این سطوح ممکن است بهصورت نیمهشفاف، مات یا با بافتهای مختلف نمایش داده شوند تا پزشک بتواند ساختارهای داخلی را بهتر تشخیص دهد.
یکی از مهمترین دستاوردهای بازسازی حجمی، امکان ایجاد «برشهای چندگانه» یا همان Multiplanar Reconstruction است. در این روش، حجم بازسازیشده به سه صفحهٔ عمود بر هم تقسیم میشود و پزشک میتواند این صفحات را در هر جهت جابهجا کند. این قابلیت، دیدی شبیه سیتیاسکن به اکو میدهد و اجازه میدهد ساختارهای قلبی در عمق بررسی شوند؛ کاری که در اکو دوبعدی تنها با حدس و تجربه ممکن بود.
بازسازی حجمی همچنین زمینهساز رندرینگ نهایی است؛ مرحلهای که در آن حجم سهبعدی به تصویری قابلمشاهده برای انسان تبدیل میشود. دستگاه با استفاده از تکنیکهایی مانند رندرینگ سطحی یا حجمی، تصویری میسازد که میتوان آن را چرخاند، بزرگنمایی کرد و از هر زاویه دید. این تصویر همان چیزی است که پزشک در مانیتور میبیند و بر اساس آن تصمیمگیری میکند.
در گذشته، بازسازی حجمی بسیار کند و محدود بود. دستگاهها نمیتوانستند حجمهای بزرگ را در زمان واقعی پردازش کنند و تصاویر سهبعدی بیشتر جنبهٔ نمایشی داشتند تا کاربرد بالینی. اما با ورود پردازندههای موازی، واحدهای پردازش گرافیکی و الگوریتمهای هوشمند، بازسازی حجمی به مرحلهای رسیده است که میتواند در کسری از ثانیه حجمهای پیچیده را بازسازی کند. اکنون پزشک میتواند قلب را در لحظه ببیند، آن را بچرخاند و حتی در حین مداخلهٔ قلبی از آن استفاده کند.
بهبیان دیگر، بازسازی حجمی همان جایی است که اکوکاردیوگرافی سهبعدی از یک فناوری صرفاً تصویربرداری، به ابزاری برای شناخت عمیق و دقیق قلب تبدیل میشود. اگر خواستی، میتوانم مرحلهٔ بعدی یعنی «رندرینگ و نمایش سهبعدی» را نیز با همین سبک و عمق توضیح دهم.

✅نمایش سهبعدی
رندرینگ و نمایش سهبعدی در اکوکاردیوگرافی، مرحلهای است که در آن دادههای حجمیِ بازسازیشده، از حالت یک ساختار خام و نامنظم، به تصویری قابلمشاهده، قابلفهم و بالینی تبدیل میشوند. اگر بخواهیم این مرحله را در یک جمله خلاصه کنیم، میتوان گفت: رندرینگ همان لحظهای است که قلب از دل دادهها «پدیدار» میشود. این مرحله، نقطهٔ اتصال میان محاسبات پیچیدهٔ دستگاه و ادراک بصری پزشک است؛ جایی که علم و هنر در کنار هم قرار میگیرند.
در آغاز این فرایند، دستگاه با یک حجم سهبعدی روبهروست که از هزاران وُکسل تشکیل شده است. هر وُکسل تنها یک مقدار شدت بازتاب دارد و هنوز هیچ شکل مشخصی از دریچهها، دیوارهها یا حفرهها در آن دیده نمیشود. رندرینگ وظیفه دارد این حجم را به تصویری تبدیل کند که ساختارهای قلبی در آن معنا پیدا کنند. نخستین گام در این مسیر، انتخاب روش رندرینگ است. دو شیوهٔ اصلی وجود دارد: رندرینگ سطحی و رندرینگ حجمی. در رندرینگ سطحی، دستگاه مرزهای ساختارها را استخراج میکند و آنها را بهصورت سطوحی پیوسته و قابلمشاهده نمایش میدهد. این روش برای نمایش دریچهها، حلقهٔ میترال و سطوح داخلی حفرهها بسیار مناسب است، زیرا خطوط و لبهها را با وضوح بالا نشان میدهد. در مقابل، رندرینگ حجمی تلاش میکند کل حجم را، با تمام لایهها و عمقهایش، بهصورت نیمهشفاف یا رنگی نمایش دهد. این روش برای مشاهدهٔ کلی قلب، بررسی جتهای نارسایی و تحلیل جریان خون کاربرد دارد.
پس از انتخاب روش رندرینگ، دستگاه باید تصمیم بگیرد که نور چگونه بر حجم بتابد، سایهها چگونه شکل بگیرند و کدام بخشها شفاف یا مات باشند. این تصمیمها تعیین میکنند که تصویر نهایی تا چه اندازه طبیعی، قابلدرک و دقیق باشد. در این مرحله، الگوریتمهای پیشرفتهٔ نورپردازی و سایهزنی وارد عمل میشوند. این الگوریتمها به دستگاه کمک میکنند تا برجستگیها، فرورفتگیها و انحنای سطوح قلب را بهگونهای نمایش دهد که چشم انسان بتواند آنها را بهدرستی تفسیر کند. بدون این نورپردازی هوشمندانه، تصویر سهبعدی چیزی جز یک تودهٔ بیروح از نقاط روشن و تاریک نخواهد بود.
یکی از مهمترین دستاوردهای رندرینگ سهبعدی، امکان مشاهدهٔ قلب از هر زاویه است. پزشک میتواند حجم را بچرخاند، آن را از بالا، پایین، جلو یا پشت ببیند و حتی وارد حفرهها شود. این قابلیت، دیدی شبیه دید جراح در اتاق عمل ایجاد میکند؛ بهویژه در بررسی دریچهٔ میترال، که نمای «روبروی جراح» به استاندارد طلایی تبدیل شده است. این آزادی در مشاهدهٔ حجم، تشخیص بسیاری از ناهنجاریها را آسانتر میکند و به پزشک اجازه میدهد ساختارهای پیچیده را بدون حدس و تفسیر ذهنی بررسی کند.
در کنار رندرینگ، مرحلهٔ «نمایش» نیز اهمیت دارد. نمایش سهبعدی تنها به معنای نشاندادن تصویر نیست؛ بلکه شامل ابزارهایی است که پزشک برای تحلیل حجم به آنها نیاز دارد. یکی از این ابزارها، برشزدن (Cropping) است. با برشزدن، پزشک میتواند بخشهایی از حجم را حذف کند تا ساختارهای پنهان آشکار شوند. این کار مانند بازکردن یک کتاب سهبعدی است؛ هر برش، لایهای جدید را نمایان میکند. ابزار دیگر، بازسازی چندصفحهای (MPR) است که حجم را به سه صفحهٔ عمود بر هم تقسیم میکند. این صفحات را میتوان در هر جهت حرکت داد تا محل دقیق ضایعه، ضخامت دیوارهها یا شکل دریچهها مشخص شود.
در نهایت، رندرینگ سهبعدی باید روان، سریع و بدون تأخیر باشد. در گذشته، دستگاهها نمیتوانستند حجمهای بزرگ را در زمان واقعی رندر کنند و تصویر سهبعدی با تأخیر یا افت کیفیت همراه بود. اما با پیشرفت پردازندهها و الگوریتمها، اکنون دستگاهها قادرند حجمهای پیچیده را در کسری از ثانیه رندر کنند. این پیشرفت، اکو سهبعدی را از یک ابزار پژوهشی به یک ابزار بالینی قدرتمند تبدیل کرده است.
بهطور خلاصه، رندرینگ و نمایش سهبعدی همان مرحلهای است که در آن قلب از دل محاسبات بیرون میآید و به تصویری زنده، قابل لمس و قابل تحلیل تبدیل میشود. این مرحله، نقطهٔ اوج فرایند تصویربرداری است؛ جایی که فناوری به خدمت تشخیص میآید و پزشک میتواند قلب را همانگونه که هست، بیواسطه و بیحدس، مشاهده کند.

📋فرآیند انجام اکو سهبعدی در کلینیک
۱. آمادهسازی بیمار
آمادهسازی صحیح بیمار، پایهٔ کیفیت تصویر در اکو سهبعدی است. برخلاف اکو دوبعدی که تا حدی به تجربه اپراتور وابسته است، در اکو سهبعدی هرگونه حرکت، آریتمی یا وضعیت نامناسب بدن میتواند باعث اعوجاج حجمی شود.
- وضعیت بدنی: بیمار باید در حالت نیمهخوابیده (semi-recumbent) قرار گیرد، معمولاً در وضعیت Left Lateral Decubitus برای اکو ترانستوراسیک.
- تنفس: در برداشتهای چندضربانی، از بیمار خواسته میشود نفس خود را برای چند ثانیه حبس کند تا از حرکت قفسه سینه جلوگیری شود.
- ECG: اتصال صحیح لیدهای الکتروکاردیوگرام ضروری است، زیرا دستگاه برای همزمانسازی ضربانها به سیگنال ECG نیاز دارد.
- آرامسازی: در بیماران مضطرب یا کودکان، استفاده از روشهای آرامسازی یا داروهای خفیف ممکن است ضروری باشد تا از حرکات ناخواسته جلوگیری شود.
- آمادگی برای TEE: در اکو مری، بیمار باید حداقل ۶ ساعت ناشتا باشد. بیحسی موضعی حلق و مانیتورینگ علائم حیاتی الزامی است.
۲. انتخاب پنجرههای استاندارد تصویربرداری
در اکو سهبعدی، انتخاب پنجرهٔ مناسب نهتنها برای وضوح تصویر، بلکه برای پوشش کامل حجم هدف حیاتی است.
پنجرههای ترانستوراسیک (TTE):
- Apical 4-chamber view: بهترین پنجره برای برداشت حجم بطن چپ و EF سهبعدی.
- Parasternal long axis: مناسب برای بررسی دریچه آئورت و ریشه آئورت.
- Subcostal view: در بیماران بستری یا با پنجرههای ضعیف توراسیک.
پنجرههای ترانسازوفاژیال (TEE):
- Mid-esophageal 4-chamber view: برای بررسی دقیق دریچه میترال و آئورت.
- Transgastric short axis: برای ارزیابی عملکرد بطن چپ از پایین.
- Bicaval view: برای بررسی دهلیز راست و وریدهای بزرگ.
انتخاب پنجره باید بر اساس هدف بالینی، وضعیت بیمار و کیفیت آکوستیک انجام شود.
۳. مراحل برداشت حجم سهبعدی
برداشت حجم سهبعدی شامل تنظیمات دقیق دستگاه، انتخاب مد تصویربرداری و کنترل شرایط فیزیولوژیک بیمار است.
انتخاب مد تصویربرداری:
- Live 3D narrow volume: برای بررسی لحظهای ساختارهای کوچک.
- 3D Zoom: برای بزرگنمایی ناحیهای خاص مانند دریچه میترال.
- Full-volume multi-beat: برای برداشت حجم کامل بطنها یا کل قلب، با رزولوشن بالا.
- 3D Color Doppler: برای بررسی جریان خون در حجم سهبعدی.
تنظیمات دستگاه:
- عمق (Depth): باید تا حدی تنظیم شود که ساختار هدف در مرکز میدان قرار گیرد.
- پهنای میدان (Sector Width): هرچه محدودتر، رزولوشن بهتر.
- Gain و TGC: باید بهگونهای تنظیم شود که بافتها واضح باشند بدون اشباع یا افت نور.
- Focus: در مرکز ساختار هدف تنظیم شود.
کنترل شرایط فیزیولوژیک:
- ECG gating: برای برداشتهای چندضربانی الزامی است.
- Breath-hold: در برداشتهای حساس به حرکت تنفسی توصیه میشود.
- تعداد ضربانها: معمولاً ۴ تا ۷ ضربان برای stitching استفاده میشود.
۴. نکات کلیدی برای بهبود کیفیت تصویر
برای دستیابی به تصویری قابلتحلیل و قابلاندازهگیری، رعایت نکات زیر ضروری است:
- تنظیم دقیق تصویر دوبعدی قبل از ورود به مد سهبعدی: تصویر ۲D باید از نظر گین، عمق و وضوح بهینه باشد.
- مرکزیت ساختار هدف در میدان تصویربرداری: اگر ساختار در حاشیه باشد، اعوجاج زاویهای رخ میدهد.
- کاهش نویز و آرتیفکتها: با تنظیم گین، کاهش حرکت بیمار و انتخاب مد مناسب.
- استفاده از مدهای بزرگنمایی برای ساختارهای کوچک: مانند لتهای دریچه یا سوراخهای بیندیوارهای.
- بررسی تصویر بازسازیشده قبل از ذخیره: تا از کامل بودن حجم و نبود آرتیفکت دوخت اطمینان حاصل شود.
- آموزش اپراتور: تجربه و مهارت تکنسین در تنظیمات و انتخاب پنجره، نقش تعیینکننده دارد.
این فرآیند، اگر با دقت و بر اساس استانداردهای جهانی انجام شود، میتواند تصویری سهبعدی با کیفیت بالا، قابلتحلیل و قابلاعتماد برای تصمیمگیری بالینی فراهم آورد.
📷زوایا و نماهای استاندارد تصویربرداری در اکوکاردیوگرافی سهبعدی
در اکوکاردیوگرافی سهبعدی، انتخاب زاویه و نمای تصویربرداری نهتنها بر کیفیت تصویر تأثیر میگذارد، بلکه تعیینکنندهٔ دقت تشخیص، امکان اندازهگیریهای کمی و قابلیت بازسازی حجمی است. برخلاف اکو دوبعدی که هر نما تنها یک برش از قلب را نشان میدهد، در اکو سهبعدی هر نما میتواند یک حجم کامل از ساختارهای قلبی را در خود جای دهد. در این فصل، نماهای استاندارد تصویربرداری در اکو ترانستوراسیک (TTE)، ترانسازوفاژیال (TEE) و سایر پنجرههای مکمل بررسی میشود.
۱. نماهای اپیکال (Apical Views)
نماهای اپیکال از ناحیهٔ نوک قلب (apex) برداشت میشوند و بهدلیل نزدیکی به بطنها و دریچه میترال، بهترین گزینه برای تصویربرداری حجمی از بطن چپ و دریچههای دهلیزیبطنی هستند.
☑️نمای چهارحفرهای (Apical 4-Chamber View)
این نما شامل بطن چپ، بطن راست، دهلیز چپ و دهلیز راست است و دریچههای میترال و تریکوسپید را در یک صفحه نشان میدهد. در اکو سهبعدی، این نما برای برداشت حجم کامل بطن چپ و محاسبهٔ EF سهبعدی بسیار مناسب است. همچنین امکان بازسازی نمای «روبروی جراح» از دریچه میترال را فراهم میسازد.

☑️نمای دوحفرهای (Apical 2-Chamber View)
در این نما، دهلیز چپ و بطن چپ دیده میشوند، بدون حضور بطن راست. این نما برای بررسی دیوارههای قدامی و تحتانی بطن چپ و ارزیابی عملکرد منطقهای کاربرد دارد. در اکو سهبعدی، میتوان حجم کوچکی از این ناحیه را با رزولوشن بالا برداشت کرد.

☑️نمای لانگاکسیس اپیکال (Apical Long Axis)
این نما مشابه نمای پاراسترنال لانگاکسیس است، اما از زاویهٔ اپیکال برداشت میشود. در آن، بطن چپ، آئورت و دریچه میترال دیده میشوند. در اکو سهبعدی، این نما برای بررسی همزمان عملکرد بطن و دریچهها مفید است.

۲. نماهای پاراسترنال (Parasternal Views)
نماهای پاراسترنال از فضای بیندندهای در کنار جناغ برداشت میشوند و بهویژه برای بررسی ساختارهای پایهای قلب مانند آئورت، دریچهها و سپتوم کاربرد دارند.
☑️نمای لانگاکسیس پاراسترنال (Parasternal Long Axis)
در این نما، بطن چپ، آئورت، دریچه میترال و قسمتی از دهلیز چپ دیده میشوند. در اکو سهبعدی، این نما برای بررسی دقیق ریشه آئورت، حلقه میترال و ارتباط بین ساختارهای پایهای قلب بسیار ارزشمند است.
☑️نمای شورتاکسیس پاراسترنال (Parasternal Short Axis)
این نما با چرخش پروب از نمای لانگاکسیس بهدست میآید و مقاطع عرضی از بطنها، دریچهها و سپتوم را نشان میدهد. در اکو سهبعدی، میتوان حجمهایی از این نما برداشت کرد که امکان بازسازی چندصفحهای (MPR) و بررسی عملکرد منطقهای را فراهم میسازد.
۳. نماهای زیرجناغی و سوپرااسترنال
این نماها در شرایط خاص، مانند بیماران بستری، کودکان یا مواردی که پنجرههای اپیکال و پاراسترنال مناسب نیستند، استفاده میشوند.
☑️نمای زیرجناغی (Subcostal View)
پروب در زیر جناغ و بالای شکم قرار میگیرد. این نما برای بررسی دهلیزها، سپتوم بیندهلیزی و ارزیابی مایع پریکارد کاربرد دارد. در اکو سهبعدی، میتوان حجمهایی از دهلیز راست و چپ برداشت کرد که برای بررسی سوراخهای بیندهلیزی مفید است.
☑️نمای سوپرااسترنال (Suprasternal View)
پروب در بالای جناغ و در ناحیهٔ گردن قرار میگیرد. این نما برای بررسی قوس آئورت و شاخههای آن استفاده میشود. در اکو سهبعدی، امکان برداشت حجم از قوس آئورت و بازسازی آناتومی عروق بزرگ فراهم است.
۴. نقش TEE سهبعدی در ارزیابی دقیق دریچهها
اکوی ترانسازوفاژیال سهبعدی (3D TEE) انقلابی در تصویربرداری از دریچههای قلبی ایجاد کرده است. بهدلیل نزدیکی مری به ساختارهای قلبی، تصاویر با رزولوشن بالا و اعوجاج کمتر بهدست میآید.
- دریچه میترال: امکان بازسازی نمای جراحی، بررسی لتها، کوردها، حلقه و نارساییها با دقت بالا.
- دریچه آئورت: ارزیابی شکل، اندازه، کلسیمگذاری و نارسایی با وضوح بالا.
- دریچه تریکوسپید و ریوی: در بیماران خاص، امکان بررسی سهبعدی ساختار و عملکرد.
- پروسیجرهای مداخلهای: مانند MitraClip، TAVR و بستهشدن سوراخهای بیندهلیزی، نیازمند تصویربرداری سهبعدی TEE در زمان واقعی هستند.
TEE سهبعدی با مدهای زنده، بزرگنمایی و داپلر رنگی، امکان هدایت دقیق پروسیجرها و ارزیابی آناتومی پیچیده را فراهم میسازد.
در مجموع، شناخت دقیق زوایا و نماهای استاندارد تصویربرداری در اکو سهبعدی، شرط لازم برای برداشت حجمهای قابلاعتماد، بازسازی دقیق و تحلیل بالینی مؤثر است.
✅پردازش و بازسازی تصاویر سهبعدی
پردازش و بازسازی تصاویر سهبعدی در اکوکاردیوگرافی، مرحلهای است که در آن دادههای حجمی خام به تصویری قابلفهم، قابلاندازهگیری و بالینی تبدیل میشوند. این فصل به چهار رکن اصلی این فرایند میپردازد: چرخش و برش حجم، بازسازی چندصفحهای، رندرینگ سطحی و حجمی، و استخراج نماهای تخصصی مانند نمای جراح. هر یک از این مراحل نقشی اساسی در تبدیل دادههای پیچیدهٔ فراصوت به تصویری شفاف و قابلتحلیل دارد.
۱. چرخش و برش حجم (Cropping)
پس از برداشت حجم سهبعدی، نخستین گام در پردازش تصویر، چرخاندن و برشزدن حجم است. حجم خام معمولاً شامل بخشهایی از بافتهای اطراف، نویز، یا ساختارهایی است که برای تحلیل بالینی ضروری نیستند. برشزدن حجم به اپراتور اجازه میدهد تا لایههای اضافی را حذف کند و ساختار موردنظر را در مرکز توجه قرار دهد.
در این مرحله، حجم سهبعدی مانند یک مکعب شفاف در نظر گرفته میشود که میتوان آن را از هر جهت چرخاند و با ابزارهای برش، بخشهایی از آن را کنار زد. این کار بهویژه در بررسی دریچهها اهمیت دارد؛ زیرا لتها، کوردها و حلقهٔ دریچه در میان بافتهای اطراف پنهان میشوند و تنها با برش دقیق حجم میتوان آنها را آشکار کرد.
برشزدن همچنین امکان ایجاد «پنجرههای دید» را فراهم میکند؛ یعنی اپراتور میتواند از میان حجم، مسیر دیدی مشابه مسیر دید جراح ایجاد کند. این قابلیت، پایهٔ استخراج نماهای تخصصی است که در ادامه به آن پرداخته میشود.
۲. بازسازی چندصفحهای (Multiplanar Reconstruction – MPR)
بازسازی چندصفحهای یکی از قدرتمندترین ابزارهای تحلیل در اکو سهبعدی است. در این روش، حجم سهبعدی به سه صفحهٔ عمود بر هم تقسیم میشود: محور طولی، محور عرضی و محور عمقی. این سه صفحه را میتوان در هر جهت حرکت داد تا ساختارهای داخلی قلب با دقت میلیمتری بررسی شوند.
MPR امکان مشاهدهٔ قلب را در مقاطعی فراهم میکند که در اکو دوبعدی قابلدستیابی نیستند. برای مثال:
- تعیین محل دقیق سوراخهای بیندیوارهای
- اندازهگیری قطر حلقهٔ دریچهها
- بررسی ضخامت دیوارهها در نواحی دور از دسترس
- تحلیل دقیق عملکرد منطقهای بطنها
در حقیقت، MPR پلی است میان تصویربرداری حجمی و تحلیل دقیق آناتومیک. بدون این ابزار، بسیاری از اندازهگیریهای سهبعدی امکانپذیر نخواهد بود.
۳. رندرینگ سطحی و حجمی
پس از برش و بازسازی، نوبت به رندرینگ میرسد؛ مرحلهای که در آن حجم سهبعدی به تصویری قابلمشاهده تبدیل میشود. دو روش اصلی رندرینگ وجود دارد:
الف) رندرینگ سطحی (Surface Rendering)
در این روش، دستگاه مرزهای ساختارهای قلبی را استخراج کرده و آنها را بهصورت سطوحی صاف و پیوسته نمایش میدهد. این روش برای بررسی:
- لتهای دریچه میترال
- حلقهٔ دریچهها
- سطوح داخلی بطنها
- نقصهای دیوارهای
بسیار مناسب است. رندرینگ سطحی تصویری شبیه مدلهای سهبعدی آناتومیک ایجاد میکند و برای تحلیل ساختارهای ظریف ایدهآل است.
ب) رندرینگ حجمی (Volume Rendering)
در این روش، کل حجم—including voxels—بهصورت نیمهشفاف یا رنگی نمایش داده میشود. این روش برای:
- بررسی کلی قلب
- تحلیل جریان خون در داپلر رنگی سهبعدی
- مشاهدهٔ جتهای نارسایی
- ارزیابی بافتهای ضخیم یا کلسیفیه
کاربرد دارد. رندرینگ حجمی عمق و بافت بیشتری به تصویر میدهد و برای نمایشهای آموزشی و جراحی بسیار جذاب است.
۴. استخراج نماهای تخصصی مانند «نمای جراح»
یکی از مهمترین دستاوردهای اکو سهبعدی، امکان استخراج نماهایی است که در اکو دوبعدی قابلدستیابی نبودند. مهمترین این نماها، نمای جراح (Surgeon’s View) است.
نمای جراح چیست؟
در این نما، دریچهٔ میترال یا آئورت از همان زاویهای دیده میشود که جراح در اتاق عمل مشاهده میکند. این نما بهویژه برای:
- ارزیابی نارسایی میترال
- برنامهریزی جراحی ترمیم دریچه
- هدایت پروسیجرهای مداخلهای مانند MitraClip
- بررسی لتها، کوردها و محل دقیق نقصها
ضروری است.
برای ایجاد این نما، اپراتور ابتدا حجم را میچرخاند، سپس با برشهای دقیق، مسیر دید را باز میکند تا سطح دریچه بهصورت کامل و بدون انسداد دیده شود. این نما بهقدری اهمیت دارد که در بسیاری از مراکز، بهعنوان استاندارد طلایی ارزیابی دریچه میترال شناخته میشود.
پردازش و بازسازی تصاویر سهبعدی، مرحلهای است که در آن دادههای خام فراصوت به تصویری زنده، دقیق و قابلتحلیل تبدیل میشود. چرخش و برش حجم، بازسازی چندصفحهای، رندرینگ سطحی و حجمی، و استخراج نماهای تخصصی، ابزارهایی هستند که اپراتور را قادر میسازند قلب را همانگونه که هست ببیند—نه در قالب حدس و تفسیر، بلکه در قالب یک مدل سهبعدی واقعی.
✅الگوریتمها و روشهای کمیسازی در اکوکاردیوگرافی سهبعدی
اکوکاردیوگرافی سهبعدی تنها یک ابزار تصویربرداری نیست؛ بلکه بستری است برای اندازهگیریهای دقیق، بازسازی هندسی واقعی قلب، و تحلیل کمی ساختارها و عملکرد قلب. برخلاف اکو دوبعدی که بسیاری از اندازهگیریها بر پایهٔ فرضهای هندسی انجام میشود، در اکو سهبعدی دادهها مستقیماً از حجم واقعی قلب استخراج میشوند. این فصل به مهمترین الگوریتمها و روشهای کمیسازی در اکو سهبعدی میپردازد.
۱. تشخیص مرزهای بافتی و سگمنتیشن (Segmentation)
سگمنتیشن، اساس تمام اندازهگیریهای کمی در اکو سهبعدی است. دستگاه باید مرز میان خون و بافت، مرز لتهای دریچه، و مرز دیوارههای بطن را تشخیص دهد. این کار با استفاده از الگوریتمهای پردازش تصویر و مدلهای هندسی انجام میشود.
الف) تشخیص مرز خون–بافت
الگوریتمها با تحلیل شدت بازتابها، نقاطی را که تغییر ناگهانی در روشنایی دارند شناسایی میکنند. این نقاط معمولاً مرز میان خون (کمانعکاس) و بافت (پرانعکاس) هستند.
ب) مدلهای فعال (Active Contours)
در این روش، یک منحنی یا سطح اولیه در حجم قرار داده میشود و الگوریتم آن را بهسمت مرز واقعی هدایت میکند. این مدلها با نیروهای داخلی (صافبودن سطح) و نیروهای خارجی (جذب به مرز واقعی) کار میکنند.
ج) الگوریتمهای یادگیری ماشین
نسل جدید دستگاهها از شبکههای عصبی برای تشخیص خودکار مرزها استفاده میکنند. این روشها:
- حساسیت کمتری به نویز دارند
- در بیماران با کیفیت تصویر پایین عملکرد بهتری دارند
- نیاز به اصلاح دستی را کاهش میدهند
سگمنتیشن دقیق، پایهٔ اندازهگیریهای حجمی و تحلیل دریچههاست.
۲. اندازهگیری حجم بطنها بدون فرض هندسی
یکی از بزرگترین مزایای اکو سهبعدی، اندازهگیری مستقیم حجم بطنها بدون نیاز به فرضهایی مانند شکل بیضوی یا استوانهای است.
چگونه انجام میشود؟
پس از سگمنتیشن:
- مرز اندوکارد بطن در تمام فریمهای قلبی مشخص میشود.
- حجم بطن بهصورت مجموع حجم وُکسلهای داخل این مرز محاسبه میشود.
- حجم پایانسیستول و پایاندیاستول بهطور مستقیم بهدست میآید.
- کسر جهشی (EF) از اختلاف این دو حجم محاسبه میشود.
مزیتها
- دقت بسیار بالاتر نسبت به روش سیمپسون دوبعدی
- عدم وابستگی به زاویهٔ تصویربرداری
- کاهش خطای ناشی از foreshortening
- امکان تحلیل عملکرد منطقهای (Regional Function)
این روش اکنون در بسیاری از راهنماهای جهانی بهعنوان استاندارد طلایی غیرتهاجمی برای اندازهگیری EF معرفی شده است.
۳. تحلیل حلقه و لتهای دریچه میترال
دریچهٔ میترال ساختاری پیچیده و سهبعدی است. اکو دوبعدی تنها برشهایی از آن را نشان میدهد، اما اکو سهبعدی امکان تحلیل کامل آن را فراهم میکند.
الف) تحلیل حلقهٔ میترال (Mitral Annulus)
الگوریتمها شکل حلقه را بهصورت سهبعدی استخراج میکنند:
- قطر قدامی–خلفی
- قطر میانی–جانبی
- ارتفاع حلقه
- Saddle shape index
- سطح حلقه
این اندازهگیریها برای برنامهریزی جراحی ترمیم میترال و انتخاب سایز رینگ بسیار حیاتیاند.
ب) تحلیل لتها
الگوریتمها لتهای قدامی و خلفی را بهصورت سهبعدی مدلسازی میکنند:
- طول لتها
- ضخامت
- سطح لت
- میزان coaptation
- محل دقیق prolapse یا flail
این تحلیل، دقت تشخیص نارسایی میترال را چندین برابر افزایش میدهد.
۴. ارزیابی شدت نارساییها با داپلر سهبعدی
داپلر سهبعدی انقلابی در ارزیابی نارسایی دریچهها ایجاد کرده است. برخلاف داپلر دوبعدی که تنها یک مقطع از جریان را نشان میدهد، داپلر سهبعدی کل حجم جریان را ثبت میکند.
الف) اندازهگیری مستقیم PISA سهبعدی
در روش دوبعدی، PISA فرض میکند که سطح همفشار کروی است؛ اما در واقعیت، شکل آن نامنظم و سهبعدی است. داپلر سهبعدی:
- سطح واقعی PISA را بدون فرض هندسی اندازهگیری میکند
- جریان مؤثر (EROA) را دقیقتر محاسبه میکند
- خطای ناشی از زاویه و شکل نامنظم را حذف میکند
ب) تحلیل جت نارسایی
داپلر سهبعدی امکان:
- اندازهگیری حجم واقعی جت
- تعیین مسیر سهبعدی جریان
- تحلیل شدت نارسایی در بیماران با جتهای پیچیده
را فراهم میکند.
ج) کاربرد در پروسیجرهای مداخلهای
در MitraClip، TAVR و ترمیمهای ترانسکاتتر:
- داپلر سهبعدی شدت نارسایی باقیمانده را دقیقتر نشان میدهد
- امکان ارزیابی لحظهای نتیجهٔ پروسیجر را فراهم میکند
الگوریتمهای کمیسازی در اکو سهبعدی، قلب این فناوری هستند. بدون آنها، حجم سهبعدی تنها یک تصویر زیبا خواهد بود؛ اما با این الگوریتمها، اکو سهبعدی به ابزاری قدرتمند برای تشخیص دقیق، برنامهریزی جراحی، ارزیابی عملکرد قلب و هدایت پروسیجرهای مداخلهای تبدیل میشود.
✅ آنچه در اکو سهبعدی دیده میشود
اکوکاردیوگرافی سهبعدی تصویری از قلب را فراتر از یک برش دوبعدی ارائه میدهد؛ این روش امکان مشاهدهٔ واقعی هندسهٔ حفرهها، انحنای دیوارهها، ساختارهای دریچهای و مسیرهای جریان خون را در قالب یک حجم فضایی فراهم میآورد. در این فصل، آنچه بهطور مشخص و بالینی در اکو سهبعدی قابلمشاهده و تحلیل است، با زبانی دقیق و ساختاریافته تشریح میشود.
👈شکل واقعی حفرهها و دیوارهها
دید سهبعدی از هندسه حفرهها
در اکو سهبعدی، بطنها و دهلیزها بهصورت حجمهای واقعی دیده میشوند؛ نه بر اساس تقریبهای هندسی ساده. این دید واقعی امکان اندازهگیری دقیق حجم، سطح و شکل حفرهها را بدون اتکا به فروض هندسی فراهم میآورد. با بازسازی حجمی میتوان انحنای دیوارهها، برجستگیها، فرورفتگیها و نواحی آکینتیک یا هایپوکینتیک را با دقت مکانی میلیمتری مشاهده کرد.
تحلیل ضخامت و حرکت دیوارهها
قابلیت بازسازی چندصفحهای (MPR) و رندرینگ حجمی اجازه میدهد تا ضخامت دیوارهها در مقاطع مختلف اندازهگیری شود و الگوی حرکت منطقهای دیوارهها در طول سیکل قلبی بررسی گردد. این اطلاعات برای تشخیص ایسکمی منطقهای، کاردیومیوپاتیها و پیگیری پاسخ به درمان حیاتی است.
شناسایی تغییرات هندسی ثانویه
تغییرات هندسی ناشی از بیماریهای ساختاری یا عملکردی—مانند اتساع بطن چپ، تغییر شکل حلقهٔ دریچه یا جابهجایی محور طولی—در اکو سهبعدی بهوضوح قابلمشاهدهاند و میتوانند مبنای تصمیمگیری درمانی و جراحی قرار گیرند.
👈آناتومی دقیق دریچهها
نمای کامل لتها و حلقهها
اکوی سهبعدی امکان نمایش همزمان لتها، کوردها، حلقه (annulus) و بافتهای پیرامونی را فراهم میآورد. این دید سهبعدی، بهویژه برای دریچهٔ میترال اهمیت دارد؛ زیرا لتها، محل اتصال کوردها و شکل حلقه را میتوان از زاویهٔ «روبروی جراح» یا هر زاویهٔ دلخواه دیگر مشاهده و اندازهگیری کرد.
ارزیابی پاتولوژیهای دریچهای
پارگی لت، کوتاهی یا طول غیرطبیعی کوردها، پرولاپس یا رترکشن لتها، رسوب کلسیم در حلقه یا لت و تداخل با ساختارهای مجاور، در تصاویر سهبعدی با وضوح بالاتری نسبت به 2D دیده میشوند. این دقت آناتومیک، برنامهریزی جراحی ترمیمی یا انتخاب روش مداخلهای را تسهیل میکند.
اندازهگیریهای عملکردی و هندسی
پارامترهایی مانند مساحت موثر دهانهٔ نارسایی (EROA)، مساحت حلقهٔ میترال در فازهای مختلف سیکل قلبی، ارتفاع لتها و انحنای سطح لتها را میتوان بهصورت کمی استخراج کرد؛ اطلاعاتی که در تصمیمگیری بالینی و پیشبینی پاسخ به ترمیم اهمیت دارند.
👈نقصهای مادرزادی و ارتباط ساختارها
شناسایی نقصهای آناتومیک
اکوی سهبعدی توانایی آشکارسازی نقصهای مادرزادی را بهصورت سهبعدی دارد؛ از سوراخهای بیندهلیزی و بینبطنی تا ناهنجاریهای پیچیدهٔ ساختاری مانند تترالوژی فالوت یا کانال آتریوونتریکولار. نمایش سهبعدی، موقعیت دقیق نقص، اندازهٔ واقعی آن و ارتباط با ساختارهای اطراف را نشان میدهد.
درک روابط فضایی بین ساختارها
در ناهنجاریهای پیچیده، شناخت روابط فضایی بین حفرهها، عروق بزرگ، دریچهها و بافتهای مجاور برای برنامهریزی جراحی یا مداخلهٔ کاتترمحور ضروری است. اکو سهبعدی این روابط را بهصورت مدلهای قابلچرخش و برشپذیر نمایش میدهد و امکان شبیهسازی مسیرهای دسترسی را فراهم میسازد.
کمک به مداخلهٔ بینابینی و جراحی
در پروسیجرهای بسته یا جراحیهای ترمیمی، اطلاعات سهبعدی دربارهٔ محل دقیق نقص، اندازهٔ آن و بافتهای نگهدارنده، راهنمایی عملی برای انتخاب ابزار، اندازهٔ پروتز یا تکنیک ترمیم است.
👈مسیرهای جریان خون و جتهای رگورژیتاسیون
نمایش جریان در فضای سهبعدی
با ترکیب دادههای داپلر رنگی سهبعدی، مسیرهای جریان خون درون حفرهها و اطراف دریچهها قابلتصویرسازیاند. این قابلیت امکان مشاهدهٔ جهت، پهنا و توزیع جریان را در یک حجم واحد فراهم میآورد، نه تنها در یک صفحهٔ دوبعدی.
شناسایی و کمیسازی جتهای رگورژیتاسیون
جتهای نارسایی دریچهای در تصاویر سهبعدی بهصورت حجمهایی با توزیع سرعت مشخص دیده میشوند. با الگوریتمهای کمیسازی میتوان حجم بازگشتی (regurgitant volume)، مساحت موثر دهانهٔ نارسایی (EROA) و نسبت بازگشتی را در یک چارچوب حجمی محاسبه کرد؛ این روشها معمولاً دقت بالاتری نسبت به برآوردهای 2D دارند، هرچند حساس به رزولوشن و آرتیفکت زاویهای هستند.
تحلیل مسیرهای پیچیده و جریانهای چندجهتی
در شرایطی که جریانها پیچیده یا چندجهتیاند—مثلاً همزمان وجود چند جت رگورژیتاسیون یا جریانهای گردابی—نمای سهبعدی امکان تفکیک و تحلیل هر مسیر را فراهم میکند و به تفکیک منشاء هر جت و برآورد سهم آن در بار همودینامیک کمک مینماید.
اکوکاردیوگرافی سهبعدی تصویری از قلب ارائه میدهد که از نظر آناتومیک و عملکردی بسیار نزدیکتر به واقعیت است؛ شکل حقیقی حفرهها و دیوارهها، آناتومی دقیق دریچهها، نقصهای مادرزادی و روابط فضایی ساختارها و مسیرهای جریان خون همگی در قالب یک حجم قابلتحلیل در دسترس قرار میگیرند. این توانمندیها، تشخیص دقیقتر، برنامهریزی درمانی هدفمندتر و هدایت بهتر پروسیجرهای مداخلهای را ممکن میسازند.
اگر مایل باشی، میتوانم این فصل را بهصورت چکلیست بالینی برای گزارشدهی یا مجموعهٔ تصاویر نمونه با توضیحات بالینی آماده کنم تا در گزارشها و آموزش بالینی استفاده شود.
✅کاربردهای بالینی و موارد تجویز اکوکاردیوگرافی سهبعدی
اکوکاردیوگرافی سهبعدی طی دو دههٔ اخیر از یک فناوری پژوهشی به ابزاری بالینی و ضروری در تشخیص، پایش و هدایت درمانهای ساختاری قلب تبدیل شده است. توانایی این روش در نمایش حجم واقعی ساختارها، اندازهگیریهای دقیق بدون فرض هندسی، و ارائهٔ نماهای تخصصی، آن را به مکملی قدرتمند برای اکو دوبعدی بدل کرده است. در این فصل، مهمترین کاربردهای بالینی و موارد تجویز اکو سهبعدی بر اساس استانداردهای جهانی (ASE، EACVI) بهصورت جامع تشریح میشود.
۱. ارزیابی بیماریهای دریچهای
☑️دریچه میترال
اکو سهبعدی در ارزیابی دریچهٔ میترال نقشی بیبدیل دارد. این روش امکان مشاهدهٔ لتها، کوردها، حلقهٔ میترال و نواحی پرولاپس یا رترکشن را با دقت بالا فراهم میکند.
- نمای جراح (Surgeon’s View) بهعنوان استاندارد طلایی برای تحلیل آناتومی میترال شناخته میشود.
- تعیین محل دقیق پرولاپس، پارگی کورد، کلسیمگذاری حلقه و اندازهگیری مساحت دهانهٔ تنگی با دقت بیشتری نسبت به 2D انجام میشود.
- در نارسایی میترال، محاسبهٔ EROA سهبعدی و حجم برگشتی با داپلر سهبعدی، ارزیابی شدت را قابلاعتمادتر میکند.
☑️دریچه آئورت
در تنگی آئورت، اکو سهبعدی امکان اندازهگیری دقیق سطح دهانهٔ دریچه (AVA) و بررسی کلسیمگذاری را فراهم میکند.
در نارسایی آئورت، حجم و مسیر جت برگشتی در فضای سهبعدی قابلتحلیل است.
☑️دریچه تریکوسپید و ریوی
اکو سهبعدی در سالهای اخیر برای ارزیابی تریکوسپید اهمیت بیشتری یافته است:
- تعیین شکل و اندازهٔ حلقه
- بررسی نارساییهای عملکردی
- تحلیل لتهای متعدد و پیچیدهٔ این دریچه
در دریچه ریوی نیز برای بیماران مادرزادی یا پس از جراحیهای ترمیمی، نمایش سهبعدی ارزشمند است.
۲. بررسی عملکرد بطنها
☑️ بطن چپ
یکی از مهمترین کاربردهای اکو سهبعدی، اندازهگیری دقیق حجمهای بطن چپ (EDV، ESV) و EF سهبعدی بدون فرض هندسی است.
- این روش نسبت به 2D خطای کمتری دارد و با MRI همبستگی بالایی نشان میدهد.
- امکان تحلیل حرکت منطقهای دیوارهها در قالب مدلهای قطعهبندی سهبعدی وجود دارد.
- در بیماران با شکل غیرطبیعی بطن (کاردیومیوپاتیها، آنوریسمها)، دقت 3D بسیار بالاتر است.
☑️ بطن راست
بهدلیل شکل پیچیدهٔ بطن راست، اندازهگیریهای 2D محدودیتهای جدی دارد.
اکو سهبعدی امکان اندازهگیری دقیق:
- حجمهای بطن راست
- EF بطن راست
- هندسهٔ اتساعیافته در نارسایی ریوی یا فشار ریوی
را فراهم میکند.
۳. تشخیص نقصهای دیوارهای
☑️نقصهای بیندهلیزی (ASD)
اکو سهبعدی در تشخیص ASD و تعیین ویژگیهای آن بسیار ارزشمند است:
- اندازهٔ واقعی سوراخ
- شکل هندسی (بیضوی، نامنظم)
- ضخامت لبهها (rims)
- ارتباط با وریدهای ریوی و دریچهها
این اطلاعات برای تصمیمگیری دربارهٔ امکان بستن سوراخ با دستگاه ضروری است.
☑️ نقصهای بینبطنی (VSD)
در VSD، اکو سهبعدی:
- محل دقیق نقص
- اندازهٔ واقعی دهانه
- ارتباط با دریچه آئورت و میترال
- مسیر جریان شنت
را با دقت بالا نشان میدهد.
☑️ نقصهای پس از سکته قلبی
پارگی دیوارهٔ بطن، آنوریسمها و شبهآنوریسمها در تصاویر سهبعدی با وضوح بیشتری دیده میشوند و امکان برنامهریزی درمانی را فراهم میکنند.
۴. برنامهریزی و هدایت مداخلات ساختاری
اکو سهبعدی، بهویژه TEE سهبعدی زنده، ابزار اصلی هدایت بسیاری از پروسیجرهای ساختاری قلب است.
☑️ TAVI (تعویض دریچه آئورت از راه کاتتر)
اکو سهبعدی در مراحل مختلف TAVI نقش دارد:
- اندازهگیری دقیق annulus و LVOT
- تعیین شکل و قطر مناسب پروتز
- بررسی موقعیت پروتز در حین استقرار
- ارزیابی نارسایی پاراوالولار پس از استقرار
☑️MitraClip و ترمیم میترال
در این پروسیجر، TEE سهبعدی ابزار اصلی هدایت است:
- تعیین محل دقیق کلیپ
- مشاهدهٔ لتها و دهانهٔ باقیمانده
- ارزیابی نارسایی باقیمانده
- جلوگیری از تنگی بیشازحد میترال
بدون 3D TEE، انجام این پروسیجر تقریباً غیرممکن است.
☑️بستن ASD و PFO
اکو سهبعدی:
- اندازهٔ دقیق سوراخ
- تعیین لبهها
- انتخاب سایز مناسب دستگاه
- هدایت استقرار دستگاه
را با دقت بالا انجام میدهد.
☑️ سایر مداخلات
- LAA closure
- پاروالولار لیک کلوزر
- ترمیم تریکوسپید با دستگاههای جدید
- والووپلاستیها
در همهٔ این موارد، نمایش سهبعدی ساختارها و ابزارها، ایمنی و دقت پروسیجر را افزایش میدهد.اکوکاردیوگرافی سهبعدی اکنون یکی از ستونهای اصلی تصویربرداری قلبی است. این روش نهتنها تشخیص دقیقتر بیماریهای دریچهای و عملکرد بطنها را ممکن میسازد، بلکه در هدایت مداخلات ساختاری نقشی حیاتی دارد. توانایی آن در نمایش حجم واقعی، اندازهگیریهای بدون فرض هندسی و ارائهٔ نماهای تخصصی، آن را به ابزاری ضروری در کلینیکهای مدرن قلب تبدیل کرده است.
✅استانداردهای بینالمللی (ASE / ESC)
استانداردهای انجمن اکوکاردیوگرافی آمریکا (ASE) و انجمن قلب اروپا (ESC/EACVI) چارچوبی یکپارچه برای انجام، تفسیر و گزارش اکوکاردیوگرافی سهبعدی فراهم میکنند. این استانداردها تضمین میکنند که تصاویر سهبعدی با کیفیت کافی برداشت شوند، اندازهگیریها قابلاعتماد باشند و گزارش نهایی برای تصمیمگیری بالینی مناسب باشد. در این فصل، اصول کلیدی این استانداردها بهصورت جامع و ساختاریافته ارائه میشود.
۱. اصول برداشت صحیح (Acquisition Principles)
برداشت صحیح حجم سهبعدی، پایهٔ تمام تحلیلهای بعدی است. استانداردهای ASE و ESC بر چند اصل بنیادین تأکید دارند:
☑️بهینهسازی تصویر دوبعدی پیش از ورود به مد سهبعدی
کیفیت تصویر 3D مستقیماً وابسته به کیفیت 2D است. بنابراین:
- عمق، گین، فوکوس و TGC باید پیش از ورود به مد سهبعدی تنظیم شوند.
- ساختار هدف باید در مرکز میدان تصویربرداری قرار گیرد.
- آرتیفکتهای حرکتی و نویز باید به حداقل برسند.
☑️ انتخاب مد مناسب تصویربرداری سهبعدی
استانداردها توصیه میکنند مد تصویربرداری بر اساس هدف بالینی انتخاب شود:
- Live 3D برای مشاهدهٔ لحظهای ساختارهای کوچک
- 3D Zoom برای دریچهها
- Full-volume multi-beat برای بطنها و حجمهای بزرگ
- 3D Color Doppler برای جریانهای پیچیده
☑️ کنترل حرکت بیمار و هماهنگی با ECG
- در برداشتهای چندضربانی، ECG gating ضروری است.
- بیمار باید در صورت امکان حبس نفس کوتاه داشته باشد.
- آریتمیها میتوانند باعث اعوجاج حجم شوند و باید در گزارش ذکر شوند.
☑️محدود کردن پهنای میدان (Sector Width)
برای افزایش رزولوشن فضایی، توصیه میشود پهنای میدان تا حد امکان محدود شود، بهویژه در بررسی دریچهها.
۲. معیارهای کیفیت تصویر (Image Quality Criteria)
استانداردهای بینالمللی کیفیت تصویر سهبعدی را بر اساس چند شاخص ارزیابی میکنند:
☑️ وضوح مرزهای بافتی
- مرزهای لتها، دیوارهها و حلقهها باید واضح و قابلتفکیک باشند.
- وجود آرتیفکتهای سایهای یا dropout باید حداقل باشد.
☑️ پوشش کامل حجم (Full Volume Coverage)
- ساختار هدف باید بهطور کامل در حجم برداشتشده قرار گیرد.
- در بررسی بطنها، apex نباید قطع یا حذف شده باشد.
- در دریچهها، کل حلقه و هر دو لت باید در حجم دیده شوند.
☑️ رزولوشن زمانی (Temporal Resolution)
- برای بطنها: حداقل ۲۰–۲۵ فریم بر ثانیه
- برای دریچهها: هرچه بالاتر، بهتر (۳۰–۴۰ فریم بر ثانیه)
- رزولوشن پایین میتواند حرکت لتها یا دیوارهها را مخدوش کند.
☑️رزولوشن فضایی (Spatial Resolution)
- voxel size باید متناسب با ساختار هدف باشد.
- رزولوشن ناکافی باعث از دست رفتن جزئیات آناتومیک میشود.
۳. توصیههای مربوط به تفسیر (Interpretation Guidelines)
تفسیر تصاویر سهبعدی باید بر اساس اصول علمی و با استفاده از ابزارهای بازسازی انجام شود.
☑️ استفاده از بازسازی چندصفحهای (MPR)
- تفسیر تنها بر اساس تصویر رندرشده کافی نیست.
- MPR باید برای تعیین دقیق مرزها، اندازهگیریها و بررسی نقصها استفاده شود.
- صفحات باید عمود بر محورهای آناتومیک تنظیم شوند.
☑️تحلیل کمی (Quantitative Analysis)
- حجم بطنها باید با روش بدون فرض هندسی محاسبه شود.
- اندازهگیری حلقهٔ دریچهها باید در فازهای مختلف سیکل انجام شود.
- در نارساییها، EROA سهبعدی و Regurgitant Volume ترجیح داده میشود.
☑️ توجه به آرتیفکتها و محدودیتها
- stitching artifact در برداشتهای چندضربانی
- dropout در لتهای نازک
- shadowing ناشی از پروتزها یا کلسیفیکاسیون
این موارد باید در تفسیر لحاظ و در گزارش ذکر شوند.
☑️ مقایسه با سایر مدالیتهها
- در موارد پیچیده، مقایسه با MRI یا CT توصیه میشود.
- اختلافات باید تحلیل و در گزارش توضیح داده شوند.
۴. ساختار گزارشدهی استاندارد (Standardized Reporting)
استانداردهای ASE و ESC ساختار مشخصی برای گزارش اکو سهبعدی پیشنهاد میکنند:
☑️اطلاعات پایه
- نوع پروب و دستگاه
- مد تصویربرداری (Live, Zoom, Full-volume)
- تعداد ضربانهای استفادهشده در stitching
- کیفیت تصویر (خوب، متوسط، ضعیف)
☑️یافتههای آناتومیک
- شکل و اندازهٔ حفرهها
- وضعیت دیوارهها
- آناتومی دریچهها (لتها، حلقه، کوردها)
- وجود نقصهای ساختاری
☑️یافتههای عملکردی
- حجمها و EF سهبعدی
- حرکت منطقهای
- شدت نارساییها با روشهای کمی
- مسیرهای جریان خون در داپلر سهبعدی
☑️تصاویر کلیدی (Key Images)
- نماهای بازسازیشده
- نمای جراح برای دریچهها
- برشهای MPR
- تصاویر داپلر سهبعدی
☑️ تفسیر نهایی و توصیهها
- جمعبندی یافتهها
- پیشنهادهای بالینی
- محدودیتهای مطالعه
- نیاز به بررسی تکمیلی (CT، MRI، TEE)
استانداردهای ASE و ESC چارچوبی دقیق برای برداشت، تفسیر و گزارش اکو سهبعدی ارائه میدهند. رعایت این استانداردها تضمین میکند که تصاویر سهبعدی نهتنها زیبا و چشمنواز، بلکه قابلاعتماد، قابلاندازهگیری و بالینی مؤثر باشند. این فصل میتواند پایهٔ یک پروتکل عملی در هر مرکز تصویربرداری قلبی باشد.
✅مزایای ارائه اکوکاردیوگرافی سهبعدی در کلینیک
ارائهٔ اکوکاردیوگرافی سهبعدی در یک مرکز تصویربرداری قلب، تنها افزودن یک تکنولوژی جدید نیست؛ بلکه ارتقای واقعی کیفیت تشخیص، دقت درمان و سطح خدمات بالینی است. این روش، با فراهمکردن تصویری حجمی و واقعی از قلب، بسیاری از محدودیتهای اکو دوبعدی را برطرف میکند و پزشک را قادر میسازد تصمیمهایی دقیقتر، سریعتر و ایمنتر اتخاذ کند. در این فصل، مزایای کلیدی ارائهٔ این خدمت در کلینیک بهصورت جامع بررسی میشود.
☑️افزایش دقت تشخیص
اکو سهبعدی با نمایش حجم واقعی قلب، امکان مشاهدهٔ ساختارها را بدون تحریف زاویهای یا وابستگی به برشهای محدود فراهم میکند.
- نمای واقعی حفرهها و دریچهها باعث میشود بسیاری از ناهنجاریها که در 2D پنهان میمانند، آشکار شوند.
- اندازهگیریهای بدون فرض هندسی—بهویژه برای حجم بطنها—خطا را به حداقل میرساند.
- نمای جراح برای دریچه میترال و آئورت، تشخیص پرولاپس، پارگی کورد، کلسیمگذاری و نارساییها را دقیقتر میکند.
- داپلر سهبعدی مسیر و حجم واقعی جتهای نارسایی را نشان میدهد، نه فقط یک مقطع دوبعدی از آنها.
نتیجه آن است که تشخیصها کمتر وابسته به تفسیر ذهنی و بیشتر مبتنی بر دادههای واقعی و قابلاندازهگیری میشوند.
☑️بهبود برنامهریزی درمان
در بسیاری از بیماریهای قلبی، تصمیمگیری درمانی به شناخت دقیق آناتومی و عملکرد قلب وابسته است. اکو سهبعدی این اطلاعات را با وضوح بالا فراهم میکند.
- در بیماریهای دریچهای، تعیین اندازهٔ حلقه، شکل لتها و محل دقیق نقص، برنامهریزی جراحی یا مداخله را بهبود میبخشد.
- در کاردیومیوپاتیها، نمایش سهبعدی دیوارهها و نواحی آکینتیک، انتخاب درمان دارویی یا مداخلهای را هدفمندتر میکند.
- در نقصهای مادرزادی، نمایش روابط فضایی ساختارها، مسیرهای دسترسی و اندازهٔ دقیق نقص، برنامهریزی جراحی را تسهیل میکند.
بهطور کلی، اکو سهبعدی به پزشک اجازه میدهد پیش از هر اقدام درمانی، تصویر کاملی از قلب داشته باشد—چیزی شبیه «پیشنمایش جراحی».
☑️کاهش نیاز به روشهای تهاجمی
یکی از مهمترین مزایای اکو سهبعدی، کاهش نیاز به روشهای تهاجمی یا پرهزینه است.
- در بسیاری از موارد، اطلاعاتی که پیشتر تنها با CT، MRI یا کاتتریزاسیون قابلدستیابی بود، اکنون با اکو سهبعدی بهصورت غیرتهاجمی بهدست میآید.
- در ارزیابی شدت نارساییها، داپلر سهبعدی میتواند جایگزین روشهای پیچیدهٔ تهاجمی شود.
- در ASD و VSD، اندازهگیریهای سهبعدی اغلب نیاز به CT یا MRI تکمیلی را کاهش میدهد.
- در بیماریهای دریچهای، تعیین دقیق آناتومی میتواند از انجام بررسیهای تهاجمی غیرضروری جلوگیری کند.
این مزیت، هم برای بیمار سودمند است و هم برای کلینیک از نظر هزینه، زمان و ایمنی.
☑️ ارتقای سطح خدمات تصویربرداری قلب
افزودن اکو سهبعدی به مجموعهٔ خدمات یک کلینیک، سطح حرفهای و علمی آن مرکز را بهطور چشمگیری ارتقا میدهد.
- افزایش اعتماد پزشکان ارجاعدهنده: پزشکان میدانند که مرکز قادر است پیچیدهترین موارد را با دقت بالا ارزیابی کند.
- افزایش رضایت بیماران: مشاهدهٔ مدل سهبعدی قلب خود، درک بیمار از بیماری و درمان را بهبود میبخشد.
- هماهنگی با استانداردهای جهانی: بسیاری از پروتکلهای جدید درمانی—بهویژه در مداخلات ساختاری—اکو سهبعدی را بهعنوان ابزار اصلی توصیه میکنند.
- افزایش توان رقابتی کلینیک: ارائهٔ این خدمت، کلینیک را در سطح مراکز پیشرفتهٔ تصویربرداری قرار میدهد.
در نهایت، اکو سهبعدی نهتنها یک ابزار تشخیصی، بلکه یک سرمایهگذاری برای ارتقای کیفیت خدمات و جایگاه علمی کلینیک است.
✅نمونه گزارش و خروجی نهایی
اکوکاردیوگرافی سهبعدی تنها زمانی ارزش بالینی پیدا میکند که خروجی آن بهصورت ساختاریافته، قابلفهم و قابلاستناد ارائه شود. این فصل به سه بخش اصلی میپردازد: ساختار گزارش استاندارد سهبعدی، نمونهٔ تصاویر و نحوهٔ توضیح آنها، و شیوهٔ ارائهٔ نتایج به بیمار و پزشک ارجاعدهنده. هدف، ایجاد یک الگوی حرفهای و هماهنگ با استانداردهای جهانی برای گزارشدهی است.
✅ساختار گزارش سهبعدی (3D Echo Report Structure)
گزارش سهبعدی باید شفاف، مرحلهبهمرحله و شامل اطلاعات کلیدی باشد. ساختار پیشنهادی مطابق با استانداردهای ASE و ESC به شرح زیر است:
☑️ اطلاعات پایه
- نوع پروب و دستگاه
- مد تصویربرداری: Live 3D، 3D Zoom، Full Volume، 3D Color
- تعداد ضربانهای استفادهشده در برداشت چندضربانی
- کیفیت تصویر: خوب / متوسط / ضعیف
- وجود آریتمی یا آرتیفکتهای حرکتی
☑️یافتههای آناتومیک
- شکل و اندازهٔ حفرهها
- وضعیت دیوارهها (حرکت، ضخامت، نواحی آکینتیک)
- آناتومی دریچهها: لتها، حلقه، کوردها، کلسیفیکاسیون
- وجود نقصهای ساختاری (ASD، VSD، آنوریسمها، پارگیها)
☑️ یافتههای عملکردی
- حجمهای بطن چپ: EDV، ESV
- EF سهبعدی
- حجمها و EF بطن راست
- شدت نارساییها با روشهای کمی (EROA، Regurgitant Volume)
- مسیرهای جریان خون در داپلر سهبعدی
☑️ تصاویر کلیدی (Key Images)
- نمای جراح از دریچهها
- برشهای MPR
- حجم بازسازیشدهٔ بطنها
- مسیر جتهای نارسایی در داپلر سهبعدی
☑️تفسیر نهایی
- جمعبندی یافتهها
- تشخیص یا تشخیصهای افتراقی
- محدودیتهای مطالعه
- توصیههای بالینی
☑️پیشنهادهای تکمیلی
- نیاز به CT یا MRI
- توصیه به TEE سهبعدی
- ارجاع برای مداخلهٔ ساختاری
✅ نمونه تصاویر و توضیحات (Sample Images & Descriptions)
در گزارش سهبعدی، تصاویر باید انتخابشده، واضح و همراه با توضیح مختصر باشند. نمونههایی از تصاویر استاندارد:
☑️ نمای جراح دریچه میترال
توضیح:
نمای سهبعدی از سطح دهلیزی دریچه میترال، لت قدامی و خلفی، محل پرولاپس یا رترکشن، و شکل حلقه.
کاربرد:
تشخیص نارسایی میترال، برنامهریزی MitraClip یا جراحی ترمیمی.
☑️حجم کامل بطن چپ
توضیح:
حجم سهبعدی بازسازیشده با مرزبندی خودکار یا دستی، همراه با نمایش EDV، ESV و EF.
کاربرد:
ارزیابی عملکرد سیستولیک بدون فرض هندسی.
☑️ بازسازی چندصفحهای (MPR)
توضیح:
سه صفحهٔ عمود بر هم که محل دقیق نقص، ضخامت دیواره یا اندازهٔ حلقه را نشان میدهند.
کاربرد:
اندازهگیری دقیق و تحلیل ساختاری.
☑️ داپلر سهبعدی
توضیح:
نمای حجمی از مسیر جت نارسایی، با نمایش توزیع سرعت در فضا.
کاربرد:
کمیسازی شدت نارسایی.
☑️ نقصهای مادرزادی
توضیح:
نمای سهبعدی از ASD یا VSD، اندازهٔ واقعی سوراخ، ضخامت لبهها و ارتباط با ساختارهای مجاور.
کاربرد:
برنامهریزی برای بستن سوراخ با دستگاه.
✅نحوه ارائه نتایج به بیمار و پزشک ارجاعدهنده
ارائهٔ نتایج باید متناسب با مخاطب باشد: پزشک ارجاعدهنده نیازمند جزئیات علمی است، اما بیمار نیازمند توضیح ساده و قابلفهم.
☑️ارائه به پزشک ارجاعدهنده
- گزارش کامل همراه با تصاویر کلیدی
- ذکر محدودیتها و کیفیت تصویر
- ارائهٔ اندازهگیریهای کمی با ذکر روش
- پیشنهادهای درمانی یا تشخیصی
- در صورت نیاز، ارسال فایل دیجیتال حجم سهبعدی
☑️ارائه به بیمار
- توضیح سادهٔ یافتهها بدون اصطلاحات پیچیده
- نمایش یک یا دو تصویر سهبعدی برای درک بهتر
- توضیح اینکه آیا یافتهها نیازمند درمان، پیگیری یا بررسی تکمیلی هستند
- پرهیز از ایجاد نگرانی غیرضروری
☑️ نسخهٔ دیجیتال
بسیاری از مراکز نسخهٔ دیجیتال شامل موارد زیر ارائه میدهند:
- تصاویر سهبعدی کلیدی
- ویدئوهای کوتاه از حجم بازسازیشده
- خلاصهٔ گزارش برای بیمار
این کار باعث افزایش رضایت بیمار و شفافیت در روند درمان میشود.
گزارش سهبعدی باید ساختاریافته، دقیق و همراه با تصاویر کلیدی باشد. ارائهٔ مناسب نتایج به پزشک و بیمار، ارزش واقعی اکو سهبعدی را آشکار میکند و نقش مهمی در تصمیمگیری بالینی دارد. این فصل میتواند الگوی استانداردی برای گزارشدهی در کلینیکهای پیشرفتهٔ تصویربرداری قلب باشد.
حتماً علیرضا — در ادامه برای هر یک از ۲۰ سؤال اکو سهبعدی، دقیقاً ۵ پاراگراف کامل ارائه میکنم.
هر پاسخ شامل ۵ پاراگراف کوتاه و منسجم است تا هم خوانایی بالا باشد و هم عمق علمی حفظ شود.
❓پرسشهای متداول
اکو سهبعدی دقیقاً چه تفاوتی با اکو دوبعدی دارد؟
اکو دوبعدی تنها برشهای تخت از قلب ارائه میدهد و اپراتور باید با کنار هم گذاشتن این برشها، شکل واقعی ساختارها را در ذهن بازسازی کند. این موضوع باعث وابستگی شدید به مهارت فرد و احتمال خطا در تفسیر میشود. در مقابل، اکو سهبعدی حجم کامل از ساختار قلب را ثبت میکند و امکان مشاهده آناتومی واقعی را فراهم میسازد. این روش شکل، اندازه و حرکت ساختارها را بدون فرضیات هندسی نشان میدهد. در نتیجه، دقت تشخیص و قابلیت تحلیل بهطور قابل توجهی افزایش مییابد.
اکو سهبعدی چگونه تصویر قلب را بازسازی میکند؟
پروب سهبعدی دادههای حجمی را در قالب هزاران نقطه (Voxel) ثبت میکند. این دادهها سپس توسط نرمافزار دستگاه به یک مدل سهبعدی بازسازیشده تبدیل میشوند. مدل ایجادشده قابلیت چرخش، برش و بزرگنمایی دارد. بازسازی هندسی باعث میشود ساختارها همانگونه که در واقعیت هستند دیده شوند. این فرآیند امکان تحلیل دقیقتری نسبت به تصاویر دوبعدی فراهم میکند.
آیا اکو سهبعدی دقت بیشتری نسبت به اکو معمولی دارد؟
در بسیاری از کاربردها، اکو سهبعدی دقت بالاتری دارد. بهویژه در اندازهگیری حجمها و EF که مستقل از فرضیات هندسی انجام میشود. این روش خطای اپراتور را کاهش میدهد و نتایج قابل تکرارتر ارائه میکند. با این حال، کیفیت تصویر به عوامل تکنیکی و مهارت اپراتور وابسته است. بنابراین همیشه جایگزین کامل اکو دوبعدی نیست، بلکه مکمل آن است.
چه بیماریهایی با اکو سهبعدی بهتر تشخیص داده میشوند؟
بیماریهای دریچهای، بهخصوص میترال و تریکوسپید، از مهمترین موارد هستند. در این بیماریها، شکل و محل نارسایی با دقت بیشتری دیده میشود. همچنین در بیماریهای مادرزادی، نقصهای دیوارهای و تودهها کاربرد زیادی دارد. ارزیابی بطن راست نیز با 3D بسیار دقیقتر از 2D انجام میشود. در مجموع، هر ساختاری که شکل پیچیده دارد با 3D بهتر دیده میشود.
آیا اکو سهبعدی برای ارزیابی دریچه میترال ضروری است؟
در بسیاری از موارد، بله. اکو سهبعدی امکان مشاهده دریچه میترال از نمای جراح را فراهم میکند. این ویژگی برای تشخیص پرولاپس، Flail، Cleft و محدودیت حرکتی بسیار ارزشمند است. در برنامهریزی مداخلات مثل MitraClip، تقریباً استاندارد طلایی محسوب میشود. بدون 3D، احتمال خطا در تعیین نوع و محل آسیب افزایش مییابد.
اکو سهبعدی در چه مواردی از اکو TEE سهبعدی بهتر است؟
اکو سهبعدی ترانستوراسیک غیرتهاجمی است و برای ارزیابی حجمها بسیار مناسب است. در مواردی که بیمار تحمل TEE ندارد، 3D TTE جایگزین خوبی است. برای بررسی آناتومی سطحی، TTE گاهی کافی است. اما برای ارزیابی دقیق دریچهها، TEE همچنان برتر است. در مجموع، انتخاب بین این دو به سؤال بالینی بستگی دارد.
یا انجام اکو سهبعدی برای بیمار دردناک است؟
خیر، هیچ تفاوتی با اکو معمولی ندارد. پروب همان پروب استاندارد است و فقط داده حجمی ثبت میشود. تنها در برخی موارد نیاز به حبس نفس چندثانیهای وجود دارد. این موضوع برای اکثر بیماران قابل تحمل است. بنابراین اکو سهبعدی یک روش کاملاً غیرتهاجمی و راحت است.
مدتزمان انجام اکو سهبعدی چقدر است؟
زمان تصویربرداری کمی بیشتر از اکو دوبعدی است. ثبت دادههای حجمی نیازمند تنظیمات دقیقتر است. گاهی چندین Acquisition برای کیفیت بهتر لازم است. بخش عمده زمان در مرحله تحلیل صرف میشود. در مجموع، زمان کل معمولاً چند دقیقه بیشتر از 2D است.
آیا اکو سهبعدی نیاز به آمادگی خاصی دارد؟
خیر، مانند اکو معمولی است. بیمار نیاز به ناشتایی یا آمادگی خاص ندارد. در Full-volume چند ضربانی، ریتم منظم کمک میکند. در بیماران با AF از Single-beat استفاده میشود. بنابراین محدودیت خاصی برای انجام آن وجود ندارد.
آیا اکو سهبعدی برای کودکان یا نوزادان قابل انجام است؟
بله، بهویژه در بیماریهای مادرزادی بسیار ارزشمند است. پروبهای مخصوص Pediatric کیفیت بهتری ارائه میدهند. در نوزادان، سرعت قلب بالا چالش ایجاد میکند. اما تکنولوژیهای جدید این مشکل را کاهش دادهاند. در مجموع، 3D ابزار مهمی در اکو کودکان است.
آیا اکو سهبعدی میتواند حجمها و EF را دقیقتر اندازهگیری کند؟
بله، این یکی از مهمترین مزایای آن است. اندازهگیری EF در 3D مستقل از مدلهای هندسی است. این موضوع باعث نزدیکی نتایج به MRI میشود. در بیماران با شکل غیرطبیعی بطن، 3D بسیار دقیقتر است. بنابراین در بسیاری از مراکز روش ارجح محسوب میشود.
آیا اکو سهبعدی برای برنامهریزی مداخله لازم است؟
در مداخلاتی مثل MitraClip تقریباً ضروری است. 3D امکان تعیین دقیق محل کلیپ را فراهم میکند. ارتفاع Leaflet و فاصله Coaptation تنها با 3D قابل ارزیابی دقیق است. بدون آن احتمال خطا افزایش مییابد. بنابراین نقش کلیدی در موفقیت مداخله دارد.
تفاوت Full-volume 3D و Live 3D چیست؟
Full-volume رزولوشن بالاتری دارد. اما معمولاً چند ضربانی است و برای AF مناسب نیست. Live 3D تکضربانی است و Frame rate بالاتری دارد. رزولوشن آن کمتر است اما برای هدایت مداخلات مناسب است. انتخاب بین این دو به هدف تصویربرداری بستگی دارد.
آیا اکو سهبعدی برای بیماران با AF قابل اعتماد است؟
در گذشته محدودیت داشت. اما اکنون تکنیکهای Single-beat کیفیت خوبی ارائه میدهند. در ارزیابی دریچهها، AF مشکل جدی ایجاد نمیکند. در اندازهگیری حجمها، دقت کمی کاهش مییابد. با این حال، نتایج قابل قبول و بالینی هستند.
محدودیتهای تکنیکی اکو سهبعدی چیست؟
مهمترین محدودیت کاهش Frame rate است. این موضوع حرکت سریع Leafletها را کمتر واضح نشان میدهد. رزولوشن فضایی نیز معمولاً پایینتر از 2D است. پنجره آکوستیک ضعیف کیفیت را کاهش میدهد. چاقی و بیماری ریوی نیز چالش ایجاد میکنند.
آیا کیفیت تصویر به دستگاه یا مهارت اپراتور وابسته است؟
بله، هر دو نقش مهمی دارند. دستگاههای جدیدتر کیفیت بسیار بهتری ارائه میدهند. اما مهارت اپراتور در Acquisition تعیینکننده است. Post-processing نیز نیازمند تجربه است. در مجموع، 3D بیش از 2D وابسته به مهارت است.
آیا اکو سهبعدی آناتومی دریچه آئورت را بهتر نشان میدهد؟
بله، بهویژه برای ارزیابی Annulus و Leafletها. این روش امکان اندازهگیری دقیق قطرها را فراهم میکند. Calcification نیز بهتر دیده میشود. در برنامهریزی TAVI بسیار مفید است. اما CT همچنان استاندارد طلایی است.
آیا اکو سهبعدی جایگزین CT یا MRI میشود؟
در بسیاری از موارد خیر. CT برای آناتومی عروقی برتر است. MRI برای حجمها و بافت قلب دقیقتر است. اما 3D Echo مزیت Real-time و بدون اشعه دارد. در برخی موارد مثل میترال حتی از CT دقیقتر است.
آیا اکو سهبعدی برای ارزیابی بطن راست مناسب است؟
بله، بطن راست شکل پیچیدهای دارد. اندازهگیری آن با 2D دشوار است. 3D امکان اندازهگیری دقیق RV volumes را فراهم میکند. در PH و بیماری مادرزادی بسیار ارزشمند است. RV EF نیز با 3D قابل اعتمادتر است.
آیا فایلهای اکو سهبعدی قابل ذخیره و تحلیل مجدد هستند؟
بله، دادههای حجمی قابل ذخیرهسازی هستند. این فایلها در نرمافزارهای مختلف قابل بازسازیاند. امکان تحلیل مجدد برای مشاوره یا آموزش وجود دارد. ارسال فایلها برای Second opinion نیز ممکن است. این ویژگی ارزش آموزشی و بالینی زیادی دارد.
🫀اکوکاردیوگرافی سهبعدی (3D) | تشخیص دقیق بیماریهای قلبی با پیشرفتهترین فناوری
اگر به دنبال بهترین متخصص اکوکاردیوگرافی سهبعدی (3D) در تهران هستید، دکتر محبوبه شیخ با سالها تجربه در زمینه تشخیص و درمان بیماریهای قلبی، خدمات تخصصی اکوکاردیوگرافی سهبعدی و چهاربعدی را با دقت بالا ارائه میدهند.
💡 اکوکاردیوگرافی سهبعدی (3D) چیست؟
اکوکاردیوگرافی سهبعدی یک روش تصویربرداری پیشرفته از قلب است که با استفاده از امواج صوتی، تصاویر دقیق و سهبعدی از ساختار و عملکرد قلب ارائه میدهد. این روش به پزشکان کمک میکند تا مشکلات قلبی را با جزئیات بیشتری بررسی کنند و بهترین راهکار درمانی را انتخاب نمایند.
🔍 کاربردهای اکوکاردیوگرافی سهبعدی:
✅ تشخیص دقیق بیماریهای مادرزادی قلب (مانند سوراخ بین دهلیزی یا بین بطنی)
✅ ارزیابی عملکرد دریچههای قلبی (تنگی یا نارسایی دریچهها)
✅ بررسی نارسایی قلبی و علل آن
✅ ارزیابی تودههای قلبی و تومورها
✅ برنامهریزی برای جراحیهای قلب با دقت بالا
✅ پایش قلب در بیماران تحت شیمیدرمانی
🌟 چرا دکتر محبوبه شیخ برای اکوکاردیوگرافی سهبعدی؟
- دارای بورد تخصصی قلب و عروق و فلوشیپ اکوکاردیوگرافی پیشرفته
- عضو انجمن اکوکاردیوگرافی ایران و آمریکا
- پزشک نمونه در سالهای ۹۶ و ۱۴۰۰
- استفاده از دستگاههای پیشرفته اکوکاردیوگرافی سهبعدی
- تجربه بالا در تشخیص و درمان بیماریهای پیچیده قلبی